Журнал "Медицинский совет" №1/2025
DOI: 10.21518/ms2025-003
Г.Р. Сагитова1, ORCID: 0000-0002-8377-6212
А.А. Антонова1, ORCID: 0000-0003-2581-0408
А.А. Екшембиев2, ORCID: 0009-0004-5205-6636
Г.А. Яманова1, ORCID: 0000-0003-2362-8979
Н.В. Сибирякова1, ORCID: 0000-0002-8344-6408
1 Астраханский государственный медицинский университет; 414000, Россия, Астрахань, ул. Бакинская, д. 121
2 Разночиновский детский дом-интернат, предназначенный для детей, имеющих психические расстройства; 416120, Россия, Астраханская область, с. Разночиновка, ул. Волжская, д. 8
Врожденные пороки развития составляют одну из актуальных медико-социальных проблем в мире. Это связано с высокой частотой встречаемости патологии и тяжестью сформированных анатомо-функциональных нарушений. Синдром Апера (Аперта) – редкий порок развития, характеризующийся синдромальным краниосиностозом, представляющий собой группу дискраний, при которых различные пороки развития и особенности оссификации костей лицевого и мозгового черепа сочетаются с аномалиями других органов и систем. До сих пор не установлена причина, приводящая к генной мутации. Заболевание возникает в результате аутосомно-доминантной мутации в гене, который локализован на длинном плече хромосомы 10, в локусе 10q26. Синдром Апера вызывается одной из двух миссенс-мутаций гена FGFR2, вовлекающей две смежные аминокислоты: S252W и P253R. Тяжелая синдактилия и умственная отсталость выражена у пациентов с мутацией P253R. Напротив, расщелины неба чаще встречаются у носителей с мутацией S252W. Синдром Апера характеризуется клинической триадой: брахицефальный череп, гипоплазия средней части лица и аномалии конечностей (синдактилия кистей и стоп). Основные диагностические признаки синдрома – акроцефалия и синдактилия пальцев кистей и стоп отмечаются в 100% случаев. Нередко у пациентов обнаруживают пороки развития головного мозга (дистопия миндалин мозжечка, стеноз яремного отверстия, арахноидальные кисты в задней черепной ямке, мальформация мозолистого тела и/или лимбических структур). Мозг увеличен в вертикальном и уменьшен в переднезаднем размерах. У всех детей отмечается косое расположение височных костей. В статье представлены данные литературы, посвященной клинике, диагностике и лечению синдрома Апера, а также клиническое наблюдение данного синдрома.
Для цитирования: Сагитова ГР, Антонова АА, Екшембиев АА, Яманова ГА, Сибирякова НВ. Синдром Апера у ребенка: случай из практики. Медицинский совет. 2025;19(1):155–160. https://doi.org/10.21518/ms2025-003.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Aper syndrome in a child: A case from practice
Gulnara R. Sagitova1, ORCID: 0000-0002-8377-6212
Alyona A. Antonova1, ORCID: 0000-0003-2581-0408
Azat A. Ekshеmbiev2, ORCID: 0009-0004-5205-6636
Galina A. Yamanova1, ORCID: 0000-0003-2362-8979
Natalya V. Sibiryakova1, ORCID: 0000-0002-8344-6408
1 Astrakhan State Medical University; 121, Bakinskaya St., Astrakhan, 414000, Russia
2 Raznochinovsky Orphanage, a Boarding School Intended for Children with Mental Disorders; 8, Volzhskaya St., Raznochinovka Village, Astrakhan Region, 416120, Russia
Congenital malformations constitute one of the most pressing medical and social problems in the world. This is due to the high incidence of pathology and the severity of the formed anatomical and functional disorders. Apert syndrome is a rare malformation characterized by syndromic craniosynostosis, which is a group of disorders in which various malformations and ossification features of the bones of the facial and cerebral skull are combined with abnormalities of other organs and systems. The cause of the gene mutation has not yet been determined. The disease occurs as a result of an autosomal dominant mutation in a gene that is localized on the long arm of chromosome 10, at the 10q26 locus. Aper syndrome is caused by one of two missense mutations of the FGFR2 gene involving two adjacent amino acids: S252W and P253R. Severe syndactyly and mental retardation are expressed in patients with the P253R mutation. On the contrary, cleft palate is more common in carriers with the S252W mutation. Aper syndrome is characterized by a clinical triad: brachycephalic skull; hypoplasia of the middle part of the face and limb abnormalities (syndactyly of the hands and feet). The main diagnostic signs of the syndrome – acrocephaly and syndactyly of the fingers and feet – are noted in 100% of cases. Often, patients are found to have malformations of the brain (dystopia of the tonsils of the cerebellum, stenosis of the jugular foramen, arachnoid cysts in the posterior cranial fossa, malformation of the corpus callosum and/or limbic structures). The brain is enlarged vertically and reduced in anteroposterior dimensions. All children have an oblique location of the temporal bones. The article presents literature data on the clinic, diagnosis and treatment of Aper syndrome, as well as clinical observation of this syndrome.
For citation: Sagitova GR, Antonova AA, Ekshеmbiev AA, Yamanova GA, Sibiryakova NV. Aper syndrome in a child: A case from practice. Meditsinskiy Sovet. 2025;19(1):155–160. (In Russ.) https://doi.org/10.21518/ms2025-003.
Conflict of interest: the authors declare no conflict of interest.
Введение
Синдром Апера является редким заболеванием, частота встречаемости синдрома в среднем составляет 1 случай на 100 000 новорожденных, причем различия поражений по половому признаку нет. Впервые данное состояние было описано в 1906 г. французским педиатром Эженом Апером [1].
Известно 5 типов синдрома Апера [2]. Первый тип – это типичный синдром Апера, включающий акроцефалию брахиофеноцефального типа, симметричной синдактилией кистей и стоп, различные аномалии внутренних органов. Синдром Крузона с оксицефалией и синдром Апера с оксицефалией и синдактилией – наиболее часто встречающиеся случаи дизостозов. Некоторые авторы объединяют эти синдромы в один – синдром Крузона – Апера (2-й тип), но симптомологическая и генетическая дифференциация опровергает это объединение [3]. При 3-м типе умеренная акроцефалия сочетается с асимметрией черепа и частичной кожной синдактилией II–III пальцев кистей и II–IV пальцев стоп. К 4-му типу относится синдром Ваарденбурга: акроцефалия, асимметрия черепа и деформация орбит, косоглазие, брахидактилия, синдактилия, ограничение подвижности коленных и локтевых суставов. Пятый тип – синдром Пфайффера – диагностируется редко: акроцефалия, частичная синдактилия кистей и стоп, сочетающаяся с характерной для этого типа аномалией первых пальцев кистей и стоп, проксимальная фаланга которых имеет трапециевидную форму, в связи с чем отмечается искривление фаланг этих пальцев в сторону локтевой кости [2].
До сих пор не установлена причина, приводящая к генной мутации [2]. Заболевание возникает в результате аутосомно-доминантной мутации в гене, который локализован на длинном плече хромосомы 10, в локусе 10q26 [4, с. 153–160]. Синдром Апера вызывается одной из двух миссенс-мутаций гена FGFR2 [5], вовлекающей две смежные аминокислоты: S252W и P253R. Тяжелая синдактилия и умственная отсталость выражена у пациентов с мутацией P253R. Напротив, расщелины неба чаще встречаются у носителей с мутацией S252W [1, 5].
Синдром Апера характеризуется клинической триадой: брахицефальный череп, гипоплазия средней части лица и аномалии конечностей (синдактилия кистей и стоп).
Основные диагностические признаки синдрома – акроцефалия и синдактилия пальцев кистей и стоп отмечаются в 100% случаев [1, 4].
Акроцефалия («башенный череп») является результатом преждевременного смыкания многих швов черепа, наиболее часто встречается коронарный краниосиностоз [5–7]. Типичные изменения лица (орбитальный гипертелоризм, экзофтальмия, косоглазие, антимонголоидный разрез глаз) связаны как с краниостенозом, так и с деформацией клиновидной кости и смещением больших крыльев этой кости кпереди [6, 8, 9]. Седловидное переносье. Нос короткий, с уплощенной спинкой и с широким выпуклым кончиком, со стенозом или атрезией хоан, носогубные складки глубокие, возможно искривление носовой перегородки [4]. Гипоплазия верхней челюсти, скуловые дуги короткие, скуловые кости мелкие. В связи с этим отмечается относительный нижнечелюстной прогнатизм [10, 11]. Рот в состоянии покоя имеет трапециевидную форму. У пациентов имеется высокое аркообразное небо, расщелина неба и небного язычка наблюдаются в 30% случаев [6, 12]. Твердое небо короче, чем в норме, мягкое небо – длиннее и толще, верхнечелюстная зубная дуга имеет V-образную форму [11]. Также может быть задержка прорезывания зубов, множественная агенезия зубов, лопатовидная форма резцов, высокая распространенность кариеса [8, 13]. Пациенты имеют низко посаженные уши и высокую вероятность снижения слуха в дальнейшем [12].
Вторым важным признаком синдрома является синдактилия кистей и стоп – практически всегда она полная, центральные три пальца подвергнуты сращению в 100% случаев [7, 8]. Проксимальные фаланги больших пальцев кистей и стоп укорочены, дистальные имеют трапециевидную форму [12]. Патология верхних конечностей всегда более выражена, чем нижних.
Со стороны внутренних органов встречаются врожденные пороки сердца и сосудов (дефекты межжелудочковой перегородки, стеноз аорты или легочного ствола), аномалии мочеполовой системы (поликистоз почек, гидронефроз, гипоспадия, неправильное положение матки) и желудочно-кишечного тракта (атрезия пищевода, трахеопищеводный свищ, анальный свищ) [12]. В литературе упоминаются пороки развития трахеи в виде отсутствия мембранозной части с формированием замкнутых хрящевых колец [12, 14]. У 2/3 пациентов преждевременное срастание между собой шейных позвонков С5 и С6 или С3 и С4 [6, 8].
Нередко у пациентов обнаруживают пороки развития головного мозга (дистопия миндалин мозжечка, стеноз яремного отверстия, арахноидальные кисты в задней черепной ямке, мальформация мозолистого тела и/или лимбических структур) [7, 8]. Мозг увеличен в вертикальном и уменьшен в переднезаднем размерах. У всех детей отмечается косое расположение височных костей.
Комплексное лечение детей с синдромом Апера – чрезвычайно сложный, многоэтапный процесс [9]. Реабилитация напрямую зависит от тяжести черепно-лицевых проявлений в результате преждевременного сращения свода черепа, швов основания черепа и средней зоны лица [8, 10, 13]. Хирургическое лечение направлено на увеличение объема черепа и коррекцию синдактилии. Возраст, в котором их проводят, остается дискуссионным, но предпочтительно проводить вмешательство как можно раньше, чтобы обеспечить нормальное развитие и функционирование мозга. В старшем возрасте ортопедические технологии направлены на улучшение качества жизни, расширение сфер самообслуживания больного [8].
Нейрохирургическое лечение включает раннюю краниоэктомию коронарного шва и фронтоорбитальную репозицию [13]. Помимо хирургического лечения патологии костей черепа, пациентам с синдактилией кистей и стоп проводят хирургическое лечение пальцев конечностей. Для формирования физиологического прикуса назначают ортодонтическое лечение [15].
Среди родителей невозможно выделить группы риска по развитию этого синдрома, а также трудно прогнозировать психическое развитие ребенка с периода новорожденности. Эти сведения имеют существенное значение для родителей, поскольку в литературе описаны случаи сочетания данного симптомокомплекса с нормальным уровнем интеллекта или с развитием олигофрении в стадии глубокой дебильности.
Диагноз обычно основывается на типичных черепно-лицевых признаках и в сложных диагностических ситуациях молекулярно-генетическое тестирование помогает установить нозологическую форму краниосиностоза [16, 17].
Ниже представляем клиническое наблюдение синдрома Апера у ребенка.
Клинический случай
Пациентка Ю., 2006 г. р. Диагноз: «Синдром Апера с синдактилией пальцев обеих кистей и обеих стоп, состояние после операций на обеих кистях».
Диагноз сопутствующий: «Симптоматическая генерализованная эпилепсия в форме атонических приступов, полная ремиссия (5 лет). Умственная отсталость тяжелой степени. Правосторонний грудопоясничный сколиоз 2-й степени. Расходящееся содружественное альтернирующее косоглазие. Двусторонний экзофтальм. Расщелина мягкого и твердого неба. Смещенная перегородка носа без нарушения дыхания».
Из анамнеза известно, что ребенок рожден от 1-й беременности, протекавшей на фоне гестоза, хламидиоза, дрожжевого кольпита, миомы матки, с угрозой прерывания на 28-й нед. На 16-й нед. беременности мать перенесла ОРИ. Роды с преждевременным излитием околоплодных вод, в тазовом предлежании, извлечена за тазовый конец, двукратное обвитие пуповины вокруг шеи плода. При рождении состояние тяжелое, обусловленное синдромом дыхательных расстройств на фоне задержки фетальной жидкости. ДН II ст. Ребенок родился с массой тела 3850 г, длиной 55 см, окружностью головы 37 см, оценка по шкале Апгар 4/7 баллов. Мать и отец состоят в неродственном браке. Профессиональных вредностей не выявлено.
Заболевание выявлено с рождения. Ребенку неоднократно проводились оперативные вмешательства с целью устранения синдактилии: в 2011 г. – устранение синдактилии 3–4 пальцев правой кисти, в 2012 г. – устранение синдактилии 2–3, 4–5 пальцев правой кисти, в 2013 г. – устранение синдактилии 1–2 и 3–4 пальцев левой кисти, в 2014 г. – устранение синдактилии 2–3, 4–5 пальцев левой кисти. С самого рождения девочка наблюдалась по поводу гипоксически-ишемической энцефалопатии; малой аномалии развития сердца, открытого овального окна; пролапса митрального клапана I ст.; гипотрофии I степени; железодефицитной анемии; левостороннего среднего гнойного отита; перенесла острую респираторную вирусную инфекцию; грипп типа А; аллергический дерматит.
При осмотре состояние расценивалось как средней степени тяжести с учетом основного и сопутствующих заболеваний. Внешний вид пациентки представлен на рис. 1.
Рисунок 1. Внешний вид пациента

Сознание было ясное, аппетит и сон не нарушены. Пищу принимала самостоятельно. Физическое развитие среднее, гармоничное. Подкожно-жировой слой развит умеренно, распределен равномерно. Речь невнятная, нарушено произношение некоторых звуков. Речевой выдох непродолжительный. Обращенную речь понимает в пределах уровня интеллекта. Фонематические процессы не сформированы. Навыки звуко-буквенного анализа не сформированы. Словарный запас беден, неточен, ограничен обиходно-бытовой тематикой. Не понимает значения многих слов. Грамматический строй не сформирован. Навыки самообслуживания сформированы частично, выполняет гигиенические мероприятия, одевается, нуждается в помощи персонала. Эмоционально незрела, примитивна, недифференцированная, склонна к аффективным реакциям. Менингеальные знаки отрицательные. Кожные покровы бледной окраски, сухие. Слизистая носа розовая, отделяемого нет. Перегородка носа искривлена вправо. Носовое дыхание свободное, отделяемого из носа нет. Слизистая оболочка задней стенки глотки розовая, влажная. Миндалины на уровне небных дужек, не спаяны с ними, чистые. Отмечается расщелина мягкого и твердого неба. Зрение нарушено, двусторонний экзофтальм. Обоняние не нарушено. Глазные щели D = S, зрачки D = S. Фотореакция прямая, содружественная. Уши AD/AS – ушные раковины правильной формы. Пальпация ушной раковины, сосцевидных отростков и козелка безболезненная. Наружные слуховые проходы чистые, барабанные перепонки серые, контуры четкие. Тургор тканей умеренный. Периферических отеков нет. Периферические лимфатические узлы не увеличены. Череп башенный, расстояние между глазами увеличено, глазные щели расположены косо: наружные углы глазных щелей наклонены книзу, наружный нос широкий. Положение головы правильное, объем движений в шейном отделе позвоночника не ограничен. Надплечья, лопатки, треугольники талии асимметричны, при наклоне туловища вперед реберный горб справа высотой до 3,0 см, паравертебральный мышечный валик в грудном отделе справа выше, чем слева, на 2,5 см, в поясничном отделе справа выше, чем слева, на 2,5 см, перекоса таза нет. Левая половина грудной клетки смещена кпереди. Верхние и нижние конечности не деформированы, не укорочены, движения в суставах осуществляются в полном объеме, за исключением пальцев кистей и стоп, объем движений в суставах которых резко сокращен (движения качательные). Синдактилия пальцев правой и левой кистей (рис. 2).
Рисунок 2. Внешний вид кистей до хирургического лечения
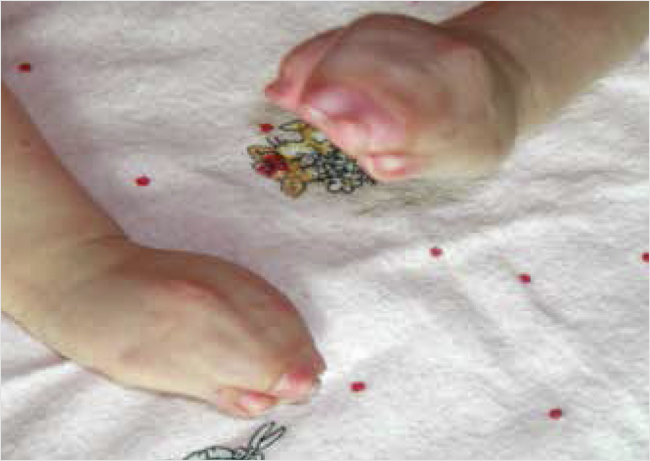
Послеоперационные рубцы на правой и левой кистях нормотрофичны (рис. 3).
Рисунок 3. Внешний вид кистей после хирургического лечения
Пальцы стоп сращены в единый конгломерат с разгибательной деформацией в плюснефаланговых суставах (около 30°) и сгибательной деформацией в проксимальных межфаланговых суставах (около 30°). Продольные своды обеих стоп выражены удовлетворительно. Дыхание без участия вспомогательной мускулатуры. Перкуторный звук легочный. Аускультативно в легких дыхание везикулярное, хрипы не выслушивались. ЧДД – 17 в мин. SpO2 – 99–98%. Область сердца визуально не изменена. Границы относительной сердечной тупости в пределах возрастной нормы. Тоны сердца ясные, ритмичные. ЧСС – 75 удара в минуту. АД на руках – 110/70 мм рт. ст. Язык чистый, влажный. Живот мягкий, безболезненный, доступен глубокой пальпации. Печень не увеличена, селезенка не пальпировалась. Симптомов раздражения брюшины не выявлено. Стул регулярный, оформленный, без патологических примесей. Мочеполовая система развита по женскому типу, правильно. Почки не пальпируются. Мочеиспускание свободное, безболезненное.
Данные общеклинических анализов крови и мочи без патологических изменений.
Показатели общепринятых биохимических параметров крови без отклонений от реферативных данных. Коагулограмма в пределах возрастной нормы.
Ребенку были проведены инструментальные исследования. По данным электрокардиограммы синусовый ритм с ЧСС – 75 ударов в минуту, нормальное положение электрической оси сердца.
На ЭЭГ в покое локальной и пароксизмальной активности не выявлено.
Учитывая наличие множественных поражений органов и систем, пациенту проведено дообследование у профильных специалистов. Так, офтальмологом выставлен диагноз: «Расходящееся содружественное альтернирующее косоглазие. Двусторонний экзофтальм»; отоларингологом: «Расщелина мягкого и твердого неба. Смещенная перегородка носа без нарушения дыхания»; неврологом: «Симптоматическая генерализованная эпилепсия в форме атонических приступов, полная ремиссия (5 лет). Умственная отсталость тяжелой степени»; травматологом-ортопедом: «Синдром Апера с синдактилией пальцев обеих кистей и обеих стоп, состояние после операций на обеих кистях. Правосторонний грудопоясничный сколиоз 2-й степени».
Обсуждение
Согласно данным литературы, синдром Апера имеет характерные клинические и рентгенологические особенности, наряду с обычными орфанными аномалиями, особенно недоразвитием средней части лица.
Дифференциальный диагноз «синдрома Апера» проводится со сходными фенотипическими проявлениями. Наличие краниосиностоза имеет место при болезни Крузона, Пфайффера, Сетре – Чотцена, Мюнке и Джексона – Вейса. Диагностическим критерием синдрома Апера считается наиболее тяжелая, тотальная синдактилия кистей и стоп. Случаи «легкого» варианта синдрома Апера достаточно сложно дифференцировать с синдромами Пфайффера. При наличии полидактилии и пороков развития внутренних органов (сердца, почек), которые встречаются в 10% случаев синдрома Апера, трудности в дифференциальной диагностике возникают с синдромом Карпентера.
Пренатальная диагностика возможна во всех триместрах беременности. Эхографическим маркером считается увеличение толщины воротникового пространства в первом триместре беременности [7]. В настоящее время при диагностике аномалий лица и конечностей применяют трехмерную ультрасонографию в поверхностном режиме, что позволяет подтвердить и уточнить диагноз. Пренатальная диагностика затруднена до тех пор, пока аномалии черепа и лица не станут более выраженными в третьем триместре [5]. При подозрении на синдром Апера во время проведения пренатальной диагностики рекомендуется проведение молекулярно-генетического исследования (биопсия ворсин хориона или амниоцентез) и обследование родителей.
Заключение
В настоящее время частота встречаемости наследственных заболеваний значительно возросла и врачу приходится порой дифференцировать соматические болезни от наследственных.
Достижения молекулярной генетики и развивающейся клеточной биологии позволяют нам понять механизмы пороков развития и открывают возможности их пренатальной диагностики. Определение фенотипа, генотипа и их корреляция крайне важны для врача.
Знание всех клинических проявлений того или иного синдрома помогает определить круг специалистов и исследований, необходимых для обследования пациентов, а также определить прогноз для жизни и здоровья.
Клиническое наблюдение представляет несомненный интерес для практикующих специалистов в связи с редкостью данного заболевания и недостаточной информированностью врачей относительно редких орфанных болезней.
Список литературы / References
Развернуть
- Климов ЛЯ, Вдовина ТМ, Курьянинова ВА, Письменова НН, Долбня СВ, Стоян МВ и др. Случай синдрома Апера у девочки. Медицинский вестник Северного Кавказа. 2012;(4):98–101. Режим доступа: https://medvestnik.stgmu.ru/. / Klimov LYa, Vdovina TM, Kuryaninova VA, Pismenova NN, Dolbnya SV, Stoyan MV et al. A case of Apert syndrome in a girl. Medical News of North Caucasus. 2012;(4):98–101. (In Russ.) Available at: https://medvestnik.stgmu.ru/.
- Маврина ЕВ, Соловьева НВ, Локотунина ВМ, Кузнецова АВ. Два наблюдения синдрома Апера. Казанский медицинский журнал. 2002;83(3):220. Режим доступа: https://www.elibrary.ru/. / Mavrina EV, Solovyova NV, Lokotunina VM, Kuznetsova AV. Two observations of Apert syndrome. Kazan Medical Journal. 2002;83(3):220. (In Russ.) Available at: https://www.elibrary.ru/.
- Колтунов ДЕ. Синдром Крузона: этиология и клинические проявления. Вопросы практической педиатрии. 2011;6(5):49–52. Режим доступа: https://www.phdynasty.ru/. / Koltunov DE. Crouzon syndrome: etiology and clinical manifestations. Clinical Practice in Pediatrics. 2011;6(5):49–52. (In Russ.) Available at: https://www.phdynasty.ru/.
- Мириева ГТ, Винокурова ЛН. Клинический случай синдрома Апера у новорожденного. В: Инновации в науке и практике: сборник статей по материалам XVI международной научно-практической конференции. В 3-х частях. Ч. 3. Инновации в науке и практике, Барнаул, 17 апреля 2019 г. Уфа: ООО Дендра; 2019. 230 с. Режим доступа: https://www.elibrary.ru/.
- Лазаревич АА, Венчикова НА, Мараховская ЭИ. Случаи диагностики синдрома Апера. Репродуктивное здоровье. Восточная Европа. 2021;11(4):496–502. Режим доступа: https://rz.recipe.by/. / Lazarevich AA, Venchikova NA, Marakhovskaya EI. Prenatal Diagnosis of Apert Syndrome. Reproductive Health. Eastern Europe. 2021;11(4):496–502. (In Russ.) Available at: https://rz.recipe.by/.
- Колтунов ДЕ, Бельченко ВА. Характеристика скелетных деформаций у пациентов с синдромами Аперта, Крузона, Пфайффера. Вопросы практической педиатрии. 2012;7(6):57–62. Режим доступа: https://www.phdynasty.ru/. / Koltunov DE, Belchenko VA. А Characteristics of skeletal deformities in patients with Apert, Crouzon, and Pfeiffer syndromes. Clinical Practice in Pediatrics. 2012;7(6):57–62. (In Russ.) Available at: https://www.phdynasty.ru/.
- Белопасов ВВ, Ткачева НВ, Сопрунова ИВ. Акроцефалосиндактилия 1-го типа (синдром Апера). Русский журнал детской неврологии. 2009;4(4):48–50. Режим доступа: https://www.elibrary.ru/. / Belopasov VV, Tkacheva NV, Soprunova IV. Acrocephalosyndactyly I type (Apert syndrome). Russkii Zhunal Detskoi Nevrologii. 2009;4(4):48–50. (In Russ.) Available at: https://www.elibrary.ru/.
- Ясонов СА. Синдромальные краниосиностозы: основные клинические проявления и современные возможности реабилитации. Педиатрия. Журнал имени Г.Н. Сперанского. 2012;91(5):108–116. Режим доступа: https://pediatriajournal.ru/. / Yasonov SA. Syndromic craniosynostosis: main clinical manifestations and modern rehabilitation options. Pediatriya – Zhurnal im G.N. Speranskogo. 2012;91(5):108–116. (In Russ.) Available at: https://pediatriajournal.ru/.
- Raposo-Amaral CE, Ghizoni E, Raposo-Amaral CA. Apert Syndrome: Selection Rationale for Midface Advancement Technique. Adv Tech Stand Neurosurg. 2023;46:245–266. doi: 10.1007/978-3-031-28202-7_13.
- Tan AP, Mankad K. Apert syndrome: magnetic resonance imaging (MRI) of associated intracranial anomalies. Childs Nerv Syst. 2018;34(2):205–216. doi: 10.1007/s00381-017-3670-0.
- Samhitha CS, Subramanyam C. Apert syndrome: a rare clinical image. Pan Afr Med J. 2023;45:24. doi: 10.11604/pamj.2023.45.24.38946.
- Benmiloud S, Chaouki S, Atmani S, Hida M. Apert syndrome. Pan Afr Med J. 2013;14:66. (In French.) doi: 10.11604/pamj.2013.14.66.2178.
- Verma S, Draznin M. Apert syndrome. Dermatol Online J. 2005;11(1):15. Available at: https://pubmed.ncbi.nlm.nih.gov/.
- Forte AJ, Lu X, Hashim PW, Steinbacher DM, Alperovich M, Persing JA, Alonso N. Airway Analysis in Apert Syndrome. Plast Reconstr Surg. 2019;144(3):704–709. doi: 10.1097/PRS.0000000000005937.
- Lopez-Estudillo AS, Rosales-Berber MA, Ruiz-Rodríguez S, Pozos-Guillén A, Noyola-Frias MA, Garrocho-Rangel A. Dental approach for Apert syndrome in children: a systematic review. Med Oral Patol Oral Cir Bucal. 2017;22(6):e660–e668. doi: 10.4317/medoral.21628.
- Al-Namnam NM, Jayash SN, Hariri F, Rahman ZAA, Alshawsh MA. Insights and future directions of potential genetic therapy for Apert syndrome: A systematic review. Gene Ther. 2021;28:620–633. doi: 10.1038/s41434-021-00238-w.
- de Angelis Ramos D, Matushita H, Cardeal DD, Nascimento CNG, Teixeira MJ. Apert syndrome without craniosynostosis. Childs Nerv Syst. 2019;35(3):565–567. doi: 10.1007/s00381-019-04050-1.






