А.Л. ТЕРЕХОВА 1, А.В. ЗИЛОВ 1, к.м.н., Г.А. МЕЛЬНИЧЕНКО 1, академик РАН, д.м.н., профессор, А.Л. ВЕРТКИН 2, д.м.н., профессор
1 Первый Московский государственный медицинский университет им. И.М. Сеченова
2 Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Сахарный диабет (СД) -- актуальная проблема современности. Чрезвычайно высокая распространенность, прогрессирующее течение, множественные тяжелые, порой инвалидизирующие, осложнения, преждевременная смертность, большие материальные затраты -- вот неполный перечень социально-экономических характеристик данного заболевания. Неизменно самыми распространенными у этой категории пациентов остаются сердечно-сосудистые заболевания (ССЗ).
СД 2-го типа среди всех типов диабета наиболее распространен. Помимо неблагоприятных последствий собственно хронической гипергликемии -- микроангио-, макроангио- и нейропатии, СД 2-го типа сопряжен также с достаточно высокой частотой ожирения, онкологических заболеваний, патологии дыхательной системы, ЖКБ, инфекционно-воспалительных поражений почек и мочевыводящих путей, доброкачественной гиперплазии предстательной железы, ТЭЛА [1--11]. Вышесказанное было также наглядно продемонстрировано в нашей работе по результатам анализа аутопсий 302 больных с СД 2-го типа [12].
Инфаркт миокарда -- одна из наиболее значимых форм сердечно-сосудистой патологии. По данным разных исследователей, он становится причиной смерти больных с СД в 18,5--39,0% случаев [12--14]. Многочисленные работы продемонстрировали, что при ИМ гипергликемия является фактором риска осложнений и неблагоприятного прогноза [14--21]. Однако в подобных исследованиях нередко не анализируются длительность и выраженность существующей гипергликемии, тип СД, сопутствующие заболевания, влияющие на течение ИМ и вероятный неблагоприятный исход у больных с СД 2-го типа [14, 15]. Таким образом, для лиц с СД 2-го типа в анамнезе перечень значимых для прогнозирования исхода ИМ факторов остается вопросом изучаемым и дискутабельным.
Цель: выявить, проанализировать факторы риска госпитальной летальности и выстроить прогностическую модель исхода у пациентов с СД 2-го типа и ИМ.
Материалы и методы: исследование ретроспективное по типу «случай -- контроль». Критериями включения были: СД 2-го типа в анамнезе и госпитализация в ГКБ №50 г. Москвы в 2009 г. по экстренным показаниям в связи с развившимся ИМ. Критерии исключения: впервые выявленная гипергликемия; другие типы сахарного диабета (СД 1-го типа, другие специфические типы СД, гестационный диабет); наличие, наряду с ИМ, другого конкурирующего/сочетанного заболевания на момент госпитализации. Материалы исследования: истории болезни и/или протоколы аутопсий по всем клиническим случаям (133 пациента), отобранным в соответствии с критериями включения и исключения. Статистическая обработка проведена с использованием программ MicrosoftExcel 2010 и IBM SPSS Statistics, версия 21. Для определения различий частот значений применяли критерий χ2, а также методы параметрической статистики (приведены среднее значение ± среднеквадратичное отклонение) или непараметрические тесты Колмогорова -- Смирнова или Манна -- Уитни (приведены медиана и 25; 75 процентили) в зависимости от характера распределения. Различия считали статистически достоверными при уровне значимости р < 0,05. Анализ взаимосвязи переменных проводился методом линейной корреляции по Пирсону. Прогностическая модель выработана методом линейной регрессии. Различающая способность методики графически представлена в виде ROC-кривой с рассчитанной площадью покрытия.
Результаты исследования: критериям включения соответствовали 133 пациента: 115 (86,5%) больных выжило и 18 (13,5%) умерло за период госпитализации. Выжившие и умершие пациенты не различались по полу: 2 (11,1%) мужчин и 16 (88,9%) женщин среди умерших, 26 (22,6%) мужчин и 89 (77,4%) женщин -- среди выживших (р ˃ 0,05). Также не различались по возрасту: 73,28 ± 11,19 года и 73,41 ± 9,31 года, умершим и выжившим соответственно (р ˃ 0,05).
У 19 выживших больных определить величину, глубину и локализацию очага поражения миокарда не представлялось возможным по различным объективным причинам: наличие на ЭКГ признаков блокады левой ножки пучка Гиса (БЛНПГ) или развитие ИМ в зоне рубцов, установленный электрокардиостимулятор. У умерших пациентов в подавляющем большинстве случаев имело место обширное поражение миокарда: 17 человек (94,4%) -- крупноочаговая форма и 1 человек (5,6%) -- мелкоочаговая форма, в отличие от выживших больных, у которых мелкоочаговая форма -- 60 человек (62,5%) -- преобладала над крупноочаговой -- 36 человек (37,5%). Различия между группами высоко достоверны (р = 0,000).

Пациенты изучаемых групп достоверно не различались по сопутствующей патологии за исключением большей частоты ампутаций нижних конечностей в анамнезе и хронической сердечной недостаточности у умерших (табл. 1). Достоверно чаще были сопряжены с летальным исходом такие осложнения, как полный AV-блок, гемотампонада и фибрилляция желудочков (ФЖ).
Больные достоверно не различались по уровням гемоглобина, гематокрита, АСТ, АЛТ, КФК, ЛДГ, калия и общего белка крови, а также ЧСС и протеинурии в общем анализе мочи при поступлении (р ˃ 0,05). Однако для пациентов, умерших от ИМ, при поступлении были характерны более низкие цифры АДсист. (112,50 ± 38,78 vs. 147,90 ± 30,64 мм рт. ст., p = 0,000) и АДдиаст. (67,78 ± 26,02 vs. 84,23 ± 15,24 мм рт. ст., р = 0,000), и напротив: более высокие показатели креатинина (274,10 ± 205,38 vs. 163,64 ± 54,37 мкмоль/л, р = 0,002), мочевины (14,85 ± 10,49 vs. 8,64 ± 3,89 ммоль/л, р = 0,000) и гликемии (12,20 ± 4,63 vs. 8,39 ± 2,16 ммоль/л, р = 0,000). Нормальные средние значения АДсист. и АДдиаст. у лиц с летальным исходом при наличии у 100% из них АГ в анамнезе, вероятно, могут свидетельствовать о тенденции к гипотонии. Дефицит необходимой информации в медицинской документации не позволил провести сравнительный анализ показателей липидного профиля, системы гемостаза, уровней Т-тропонина, креатинфосфокиназы МВ (КФК-МВ).
Пациенты указанных групп достоверно не различались по исходной (до госпитализации) сахароснижающей терапии (ССТ): в целом 28 человек (21,05%) получали диетотерапию, 75 человек (56,4%) -- пероральные сахароснижающие препараты (ПССП), 22 человека (16,5%) -- инсулинотерапию и 8 человек (6,5%) -- комбинацию инсулина с ПССП. Сахароснижающая терапия, проводимая в отделении кардиологической реанимации, также не влияла на конечный исход заболевания: из общего числа пациентов у 52 человек (39,7%) -- диетотерапия, 74 человек (56,5%) -- инсулинотерапия, 3 человек (2,3%) -- ПССП, 2 человек (1,5%) -- комбинация инсулина с ПССП. Согласно данным медицинской документации, у больных обеих групп за период пребывания в стационаре гипогликемий зафиксировано не было.
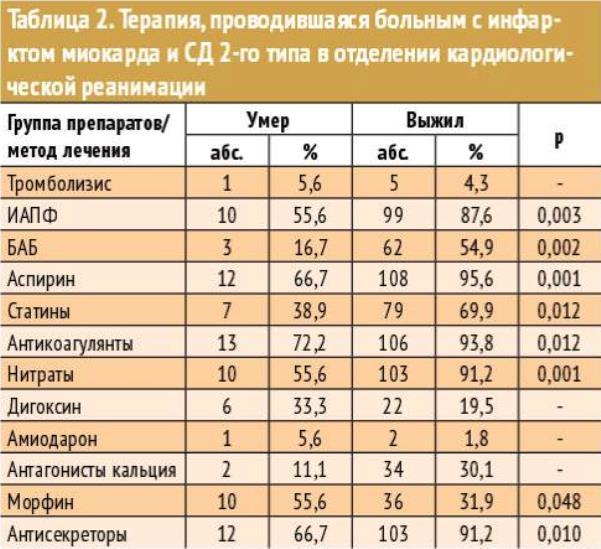
Проанализировать сопутствующую терапию, получаемую пациентами до госпитализации, не представилось возможным в связи с дефицитом необходимой информации в медицинской документации. При анализе терапии, проводимой больным после их госпитализации в отделении кардиологической реанимации, было выявлено, что пациентам, исход заболевания (ИМ) у которых впоследствии оказался неблагоприятным, достоверно реже назначались ИАПФ, β-адреноблокаторы, аспирин, статины, антикоагулянты (гепарин, низкомолекулярные гепарины), нитраты и антисекреторные препараты (Омепразол, Ранитидин и др.) (табл. 2). Вероятно, это было обусловлено такими факторами, как артериальная гипотензия при поступлении, явления сердечной недостаточности и наличие нарушений сердечной проводимости, ограничивавшими показания к ряду групп препаратов, а также кратковременностью пребывания в стационаре (вследствие летального исхода).
При корреляционном анализе выделены факторы, достоверно связанные с неблагоприятным исходом у больных СД 2-го типа и ИМ. Выявленные факторы учтены в ходе многофакторного анализа по методу линейной регрессии: наиболее значимые из них вошли в выстроенную модель прогноза летальности (табл. 3). При анализе связи неблагоприятного исхода у больных с СД 2-го типа и ИМ с уровнем гликемии при поступлении было выявлено, что летальность достоверно больше при гликемии ˃8,0 ммоль/л (8,23 vs. 22,9%, p = 0,018) и положительно коррелирует с дальнейшим ростом гликемии (r = 0,545, p = 0,000). Однако существенное прогностическое значение в рамках моделирования имеет «cut-off» на уровне 11,0 ммоль/л, меньше которого летальность составляет до 7,3%, а при ≥11,0 ммоль/л резко возрастает до 41,7% (р = 0,0001). В связи с установленным фактом для повышения качества прогноза методом ручной линеаризации была получена преобразованная переменная «гликемия при поступлении 11», способная принимать два значения: «0» -- если уровень глюкозы составил ˂11,0 ммоль/л, и «1» -- если гликемия была ≥11,0 ммоль/л.

В представленной модели мочевина крови задавалась в ммоль/л, АД систолическое -- в мм рт. ст.; гликемия при поступлении 11 вносилась как «0», если была ˂11,0, и «1» -- если была ≥ 11,0 ммоль/л; характер поражения миокарда (обширность и глубина): «0» если определить это не представляется возможным по объективным причинам, «1» -- если мелкоочаговый ИМ, «2» -- если крупноочаговый ИМ и «3» -- если трансмуральный ИМ. Хроническая сердечная недостаточность задавалась как «0» при отсутствии ее признаков и как «1» -- при их наличии. Под нарушениями сердечной проводимости (не фатальные) понимали постоянное/преходящее нарушение проведения через АV-соединение I-IIст., нарушение проведения по ножкам и ветвям пучка Гиса, выявляемые на ЭКГ исходно при поступлении («1») или развивавшиеся в динамике («2»); отсутствие указанных изменений на ЭКГ обозначалось как «0».
В соответствии с таблицей 3 получена формула для расчета прогноза: ПРОГНОЗ = 1,0363 + (-0,1607 * характер поражения миокарда) + (-0,1793 * гликемия при поступлении 11) + (0,0019 * АД систолическое) + (-0,0118 * мочевина крови при поступлении) + (-0,1353 * нарушения проводимости) + (-0,1217 * ХСН).
В качестве примера возьмем воображаемого пациента с СД 2-го типа, у которого развился мелкоочаговый ИМ («1») с постоянной AV-блокадой I степени («1»), но без данных анамнеза и клинических признаков ХСН («0»); при этом мочевина крови исходно 8,3 ммоль/л, гликемия при поступлении 12,0 ммоль/л («1»), АД систолическое при поступлении 130 мм рт. ст. Прогноз для данного пациента составит 1,0363 + (-0,1607 * 1) + (-0,1793 * 1) + (0,0019 * 130) + (-0,0118 * 8,3) + (-0,1353 * 1) + (-0,1217 * 0) = 0,710.
При последующей статистической обработке была рассчитана новая переменная -- «округленная величина прогноза», по итогам сопоставления которой с исходами были выделены 4 диапазона величины прогноза. Таким образом, полученная величина может быть переведена в вероятность летального исхода в соответствии с таблицей 4, согласно которой вероятность смерти описанного нами виртуального пациента составит 11,11%.

Различающая способность разработанной методики прогнозирования показана на рисунке 1. Площадь покрытия составляет 0,974, что характеризует методику как весьма качественную: повышение чувствительности сопряжено с сохранением достаточно высокой специфичности. Эффективность (однозначность вывода) и надежность (безошибочность вывода) методики также оказались равнозначно высокими и составили 96,2% (126 случаев из 131).
Обсуждение результатов
Из всех факторов, проявивших свое значимое влияние на прогноз летальности, величина и глубина поражения миокарда, наличие ХСН и в определенной степени уровень АД систолического по существу являются предикторами и маркерами функциональных компенсаторных возможностей интактного миокарда. Наличие СД как такового обусловливает высокие риски наличия диабетической кардиомиопатии, диастолической дисфункции левого желудочка и при прогрессировании процесса -- ХСН. Вышеперечисленное, сочетаясь с обширным и/или глубоким поражением миокарда, в совокупности определяет сниженный функциональный резерв левого желудочка и, следовательно, неблагоприятный прогноз выживаемости после ИМ. Нарушения проводимости сердца, регистрируемые исходно, являются, вероятно, отражением предсуществующего кардиосклероза (на фоне ИБС) и/или кардиомиопатии. Отсюда понятен вклад данного фактора также в снижение компенсаторных возможностей непораженного инфарктом миокарда и негативное влияние на прогноз.
Результаты нашей работы подтвердили, что уровень глюкозы крови в остром периоде ИМ является независимым предиктором неблагоприятного прогноза на госпитальном этапе. Повышенная летальность (8,23 vs. 22,9%, p = 0,018) ассоциировалось с гликемией при поступлении >8,0 ммоль/л, положительно коррелировала с дальнейшим ростом гликемии (r = 0,545, p = 0,000) и резко увеличивалась при уровне глюкозы крови ≥11,0 ммоль/л (до 41,7%, р = 0,0001). При гликемии ≥11,0 ммоль/л значимо возрастала частота таких осложнений, как фибрилляция желудочков (0,9 vs. 16,7%, p = 0,0037; RRФЖ при гликемии ≥11,0 = 18,17, 95% CI 2,011--425,632) и отек легких (ОЛ) (6,4 vs. 25,0%, p = 0,013; RRОЛ при гликемии ≥11,0 = 3,89, 95% CI 1,23--11,8). Хотя на данный момент общепринятый целевой диапазон гликемии у больных с острым коронарным синдромом окончательно не определен, анализ полученных нами данных позволяет выделить две значимые пороговые величины гликемии при поступлении у пациентов с СД 2 в анамнезе -- 8 и 11 ммоль/л, за верхними рамками которых возрастает риск осложнений и внутрибольничная летальность. Данные значения приближаются к цифрам, которые приняты обоснованными целевыми для большинства больных по результатам клинических исследований: гликемия в течение суток 6,5--7,8 ммоль/л с допустимым периодическим повышением до 10,0 ммоль/л [14, 16, 17, 21]. Таким образом, гипергликемия при поступлении в стационар у больных с сочетанием ИМ и СД 2-го типа ассоциируется с фатальными осложнениями, возникающими в основном в остром периоде ИМ, а также утяжеляет последующее течение ИМ в остром и подостром периоде [15]. Существенный вклад такого фактора, как азот мочевины крови, в выстроенную нами прогностическую модель исхода еще раз доказывает, что почечная дисфункция ассоциируется с увеличением риска смерти при остром коронарном синдроме [14, 22--26].
В своей работе Е.И. Панова среди факторов, ассоциированных с неблагоприятным исходом у больных с ИМ и диабетом, выделяет пожилой возраст, длительный (>10 лет) коронарный анамнез, а также наличие диабетической нефропатии II-III стадий и гипергликемии при госпитализации [14]. Deborah Chyun и соавт. (2002) в своем исследовании выявили ухудшение прогноза при существовании следующих условий: пожилой возраст, предшествующая НК, атеросклеротическое поражение периферических артерий, сниженное АД систолическое, неопределенная локализация очага поражения миокарда и др. [14, 27]. Возраст не стал значимым прогностическим фактором в нашей работе, вероятно, в связи с тем, что выборка была почти на 90% представлена лицами пожилого и старческого возраста. При этом, так или иначе, проявилась роль почти всех остальных факторов из вышеперечисленных.
Объективный взгляд на совокупность выделенных нами значимых факторов прогноза подводит к серьезному практическому заключению: на этапе уже развившегося ИМ клиницист не в состоянии коренным образом повлиять на большую часть из них. Хроническая НК, нарушение сердечной проводимости, азотемия в таком случае предстают перед практическим врачом как данность, при которой порой лечебные усилия вынужденно сводятся лишь к поддержанию жизненно важных функции в условиях сниженных компенсаторных возможностей интактного миокарда и наличия нефропатии. Нередко подобные ситуации влекут также обоснованные ограничения применения ряда прогностически важных при ИМ групп лекарственных препаратов [21]. Потенциально модифицируемыми остаются 2 позиции -- размер очага поражения миокарда и уровень гликемии. Обширность некроза может быть уменьшена при своевременном проведении тромболизиса. Этому, однако, зачастую противостоит множество факторов: атипичное течение ИМ и низкая медицинская культура населения, приводящие к поздней госпитализации, а также наличие других противопоказаний к тромболизису (помимо сроков проведения) у пациентов старшего возраста и/или отсутствие возможностей к его проведению в условиях конкретного лечебного учреждения. Отсюда ясно, что реальные возможности влиять на обсуждаемый фактор весьма ограниченны, а в распоряжении клинициста остаются буквально гликемический контроль и мониторинг/поддержание жизненноважных функций с расчетом на выносливость адаптивных систем организма. Таким образом, напрашивается вывод, что ощутимо «улучшать» прогноз исхода ИМ при СД 2-го типа можно, лишь предупреждая его (ИМ) развитие посредством своевременной диагностики и коррекции факторов кардиоваскулярного риска и рационального лечения сахарного диабета.
Выводы
Инфаркт миокарда при сахарном диабете сопряжен с высокой летальностью на госпитальном этапе. Повышенный риск внутрибольничной смерти пациентов с СД 2-го типа и ИМ ассоциирован с низким функциональным резервом интактного миокарда на фоне адекватно неконтролируемой гипергликемии и предсуществующих артериальной гипертензии, ИБС и/или диабетической кардиомиопатии, а также почечной дисфункцией. В этой связи своевременная и адекватная коррекция факторов сердечно-сосудистого риска, нормализация гликемии или профилактика развития СД и его осложнений являются основными задачами по снижению летальности от кардиоваскулярной патологии у больных сахарным диабетом 2-го типа.
Литература
1. Benfield T, Jensen JS, Nordestgaard BG: Influence of diabetes and hyperglycaemia on infectious disease hospitalisation and outcome. Diabetologia, 2007, 50: 549–554.
2. O'Meara ES, White M, Siscovick DS, Lyles MF, Kuller LH: Hospitalization for pneumonia in the Cardiovascular Health Study: incidence, mortality, and influence on longer-term survival. J Am Geriatr Soc., 2005, 53: 1108–1116.
3. Титова Е.А. Особенности течения и лечения хронической обструктивной болезни легких в сочетании с сахарным диабетом: автореф. дис. … д-ра мед. наук. 2009.
4. Ghulam HB, Mukhtiar HJ, Chandra M et al. Frequency and pattern in patients with diabetes mellitus. Professional Med, 2011, 18(3): 466-469.
5. Huxley R, Ansary-Moghaddam A, Berrington de González А, Barzi F, Woodward M. Type-II diabetes and pancreatic cancer: a meta-analysis of 36 studies. British Journal of Cancer. 2005, 92: 2076–2083.
6. Larsson SC, Orsini N, Wolk A. Diabetes Mellitus and Risk of Colorectal Cancer: A Meta-Analysis. Oxford Journals Medicine. JNCI. J Natl Cancer Inst., 2005, 97(22): 1679-1687.
7. Кособян Е.П., Смирнова О.М. Современные концепции патогенеза неалкогольной жировой болезни печени. Сахарный диабет. 2010, 1: 55-64.
8. Shakil A, Church RJ, Rao SS Gastrointestinal Complications of Diabetes Am. Fam. Physician. 2008, 15 (12): 1697-1702.
9. Parsons JK, Carter HB, Partin AW, Windham BG, Metter EJ, Ferrucci L, Landis P, Platz EA. Metabolic factors associated with benign prostatic hyperplasia. J Clin Endocrinol Metab 2006, 91(7): 2562–8.
10. Gibson TN, Char G Causes Of Death At Autopsy In Hospitalized Adult Patients With Diabetes Mellitus: A Study From A Developing Country. The Internet Journal of Pathology 2007, 6(1).
11. Joron GE, Laryea E, Jaeger D, Macdonald L Cause of death in 1144 patients with diabetes mellitus: an autopsy study. CMAJ April 1986, 134(7): 759–764.
12. Терехова А.Л., Зилов А.В., Верткин А.Л., Мельниченко Г.А. Сопутствующая патология и основные причины смерти больных с сахарным диабетом 2 типа по результатам аутопсий. Сахарный диабет. 2011, 4: 61-64.
13. Александров А.А., Бондаренко И.З., Кухаренко C.С., Ядрихинская М.Н., Мартьянова И.И., Соляник Ю.А., Дроздова Е.Н., Майоров А.Ю. Сахарный диабет и ишемическая болезнь сердца: поиски решения. Сахарный диабет. 2005, 3: 34-38.
14. Панова Е.И. Корригируемые и некорригируемые факторы неблагоприятного течения и отдаленных исходов инфаркта миокарда у больных сахарным диабетом 2 типа: автореф. дис. … д-ра мед. наук. 2009.
15. Рудакова Л.Е., Беляева Ю.Б., Рахматуллов Ф.К., Бондаренко Л.А., Ушакова С.В. Особенности течения фатального инфаркта миокарда у больных сахарным диабетом 2 типа. Медицинские науки. Клиническая медицина. 2011, 2 (18): 117-127.
16. Malmberg K et al. for the DIGAMI 2 Investigators. Intense metabolic control by means of insulin in patients with diabetes mellitus and acute myocardial infarction (DIGAMI 2): effects on morbidity and mortality. Eur Heart J 2005, 26: 650–661.
17. Дедов И.И., Шестакова М.В. Алгоритмы специализированной медицинской помощи больным сахарным диабетом. 6-й вып. М., 2013.
18. Christina H. Wei, Sheldon E. Litwin Hyperglycemia and Adverse Outcomes in Acute Coronary Syndromes: Is Serum Glucose the Provocateur or Innocent Bystander? Diabetes. 2014, 63: 2209–2212. DOI: 10.2337/db14-0571.
19. Wahab NN, Cowden EA, Pearce NJ, Gardner MJ, Merry H, Cox JL. Is blood glucose an independent predictor of mortality in acute myocardial infarction in the thrombolytic era? J Am Coll Cardiol. 2002, 40: 1748 –1754.
20. ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. European Heart Journal. 2014, 35 (27) http://dx.doi.org/10.1093/eurheartj/ehu076.
21. Всероссийское научное общество кардиологов. Рекомендации по лечению острого коронарного синдрома без стойкого подъема сегмента ST. Рациональная фармакотерапия в кардиологии, 2012, прил. 2: 2-64.
22. Национальные рекомендации по кардиоваскулярной профилактике. Кардиоваскулярная терапия и профилактика. 2011, 10(6), 2.
23. Шамхалова М.Ш. Патология почек у больных с сахарным диабетом 2 типа: сосудистые, токсические и гормональные аспекты: автореф. дис. … д-ра мед. наук. 2008.
24. Hasdai D, Behar S, Wallentin L et al. A prospective survey of the characteristics, treatments and outcomes of patients with acute coronary syndromes in Europe and the Mediterranean basin; the Euro Heart Survey of Acute Coronary Syndromes (Euro Heart Survey ACS). Eur Heart J 2002, 23: 1190–1201.
25. Goldenberg I, Subirana I, Boyko V et al. Relation between renal function and outcomes in patients with non-ST-segment elevation acute coronary syndrome: real-world data from the European Public Health Outcome Research and Indicators Collection Project. Arch Intern Med 2010, 170: 888–895.
26. Szummer K, Lundman P, Jacobson SH et al. Relation between renal function, presentation, use of therapies and in-hospital complications in acute coronary syndrome:
data from the SWEDEHEART register. J Intern Med., 2010, 268: 40–49.
27. Deborah Chyun et al. Сardiac outcomes after myocardial infarction in elderly patients with diabetes mellitus. American Journal of Critical Care, 2002, 11: 504-519.
Источник: Медицинский совет, № 2, 2015








