Журнал "Медицинский совет" №2/2023
DOI: 10.21518/ms2023-027
А.Л. Пирузян1, ORCID: 0000-0001-8039-8474
Д.Р. Мильдзихова1, ORCID: 0000-0002-5896-7455
Л.Р. Сакания1,2, ORCID: 0000-0003-2027-5987
И.М. Корсунская1, ORCID: 0000-0002-6583-0318
1 Центр теоретических проблем физико-химической фармакологии РАН; 109029, Россия, Москва, ул. Средняя Калитниковская, д. 30
2 Московский научно-практический центр дерматовенерологии и косметологии; 127473, Россия, Москва, ул. Селезневская, д. 20
Старение, и в частности возрастные изменения кожи, все больше беспокоят человечество, особенно учитывая увеличение продолжительности жизни. Старение кожи – это не просто проблема дряблости покровов, скорее, это комплексная проблема, обусловленная множеством факторов, – от дефицита иммунитета до образа жизни, влияющего как на сохранение барьерной функции кожи, так и благополучие стволовых клеток, поддерживающих орган. С течением времени меняется структура и количество липидов в роговом слое, эпидермис становится тоньше, что приводит к снижению барьерной функции кожи. Также эти изменения становятся причиной увеличения потери трансэпидермальной жидкости. В дерме процессы, связанные со старением, ведут к потери эластичности кожных покровов и также снижению гидратации. Повышение уровня цитокинов и гистамина в коже может спровоцировать зуд и расчесывание, что приведет к дальнейшему усилению кожного воспаления. Все это может проявляться выраженным ксерозом, шелушением и другими неприятными симптомами. Победить старение невозможно, однако минимизировать его проявления – достижимая цель. Наш опыт позволяет рекомендовать средства ухода с выраженными питательными и увлажняющими свойствами на основе пантенола, пребиотиков и пробиотиков, натрия гиалуроната и натурального комплекса гликоцерамидов, холестерина и фосфолипидов. Пантенол обладает регенерирующим и смягчающим действием, питает и снимает раздражение, способствует увеличению прочности и коллагеновых волокон. Натрия гиалуронат отвечает за глубокое увлажнение кожи, улучшение ее тонуса и упругости. Комплекс церамидов восполняет нехватку липидов и способствует удержанию влаги в роговом слое. Регулярный уход помогает минимизировать ксероз, зуд, чувство стянутости кожи и сохранить качество жизни у возрастных пациентов.
Для цитирования: Пирузян А.Л., Мильдзихова Д.Р., Сакания Л.Р., Корсунская И.М. Возрастные изменения кожи: причины и последствия. Медицинский совет. 2023;17(2):8–12. https://doi.org/10.21518/ms2023-027.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Aging changes in skin: causes and effects
Anastas L. Piruzyan1, ORCID: 0000-0001-8039-8474
Dzerassa R. Mildzikhova1, ORCID: 0000-0002-5896-7455
Luiza R. Sakaniya1,2, ORCID: 0000-0003-2027-5987
Irina M. Korsunskaya1, ORCID: 0000-0002-6583-0318
1 Center for Theoretical Problems of Physico-Chemical Pharmacology RAS; 30, Srednyaya Kalitnikovskaya St., Moscow, 109029, Russia
2 Moscow Scientific and Practical Center of Dermatovenerology and Cosmetology; 20, Seleznevskaya St., Moscow, 127473, Russia
Aging, and in particular aging changes in skin, are increasingly giving cause for concern to the mankind, especially given the fact that the life expectancy is extending. Skin aging is not only a problem that concerns skin sagginess, but rather it is a complex problem caused by many factors, from immune deficiency to the lifestyle, which affects both the maintenance of the skin’s barrier function and the well-being of the stem cells that support the organ. The structure and amount of lipids in the stratum corneum changes over time, the epidermis becomes thinner, which leads to decreased barrier function of the skin. These changes also cause increased loss of transepidermal fluid. The aging-associated processes in the dermis lead to a loss of skin elasticity and a decrease in hydration. The increased levels of cytokines and histamine in the skin can cause itching and scratching, which will lead to a further increase in skin inflammation. All this can be manifested by severe xerosis, peeling and other unpleasant symptoms. It is impossible to defeat aging, but to minimize its manifestations is an achievable goal. Our experience allows us to recommend care products with pronounced nutritional and moisturizing properties, which contain panthenol, prebiotics and probiotics, sodium hyaluronate and a natural complex of glycoceramides, cholesterol and phospholipids. Panthenol has a regenerating and softening effect, nourishes and relieves irritation, contributes to the increasing strength of collagen fibres. Sodium hyaluronate is responsible for deep hydration of the skin, improving its tone and elasticity. The ceramide complex compensates for the lack of lipids and helps to retain moisture in the stratum corneum. Regular care helps to minimize xerosis, itching, skin tightness and maintain quality of life in aging patients.
For citation: Piruzyan A.L., Mildzikhova D.R., Sakaniya L.R., Korsunskaya I.M. Aging changes in skin: causes and effects. Meditsinskiy Sovet. 2023;17(2):8–12. (In Russ.) https://doi.org/10.21518/ms2023-027.
Conflict of interest: the authors declare no conflict of interest.
Введение
Хотя в некоторых культурах возраст ассоциируется с мудростью и поэтому вызывает уважение, в западных обществах, постоянно ищущих молодость, старение чаще всего является источником беспокойства. Поскольку кожа находится в непосредственном контакте с окружающей средой, она подвергается воздействию внешней среды, в частности ультрафиолетовых (УФ) солнечных лучей, ответственных за фотостарение, которое ускоряет процессы старения. На самом деле кожа, как зеркало, отражает физиологическую целостность всех наших жизненных функций. Этот «сторожевой» орган, пронизанный обширной сетью кровеносных сосудов и нервных волокон, состоит из трех отдельных и наложенных друг на друга слоев: эпидермиса, дермы и гиподермы. На поверхности нашей кожи со временем появляются видимые проявления старения, такие как морщины, пятна, сухость кожи, потеря эластичности или расширение мелких кровеносных сосудов. С увеличением продолжительности жизни борьба со старением и его последствиями стала серьезной общественной проблемой и является серьезной научной и экономической задачей.
Физиологические механизмы старения кожи
Роговой слой, самый внешний слой эпидермиса, состоит из корнеоцитов, расположенных в виде компактных слоев, встроенных во внеклеточный матрикс, полученный из ламеллярных гранул, образующих богатые липидами мембраны. Толщина рогового слоя может изменяться на протяжении всей жизни и может утолщаться в ответ на различные повреждения или воспалительные состояния. Тем не менее исследования показали, что общая толщина рогового слоя молодой и старой кожи существенно не различается. Повреждения этого слоя происходят значительно медленнее, чем в молодой коже, и проницаемость для некоторых веществ изменяется [1]. Недавнее исследование, посвященное изучению биохимических характеристик рогового слоя в стареющей коже на защищенных от солнца участках, показало, что с возрастом происходит уплотнение этого слоя с увеличением клеточной сплоченности из-за изменения структуры липидов и снижения концентрации межклеточных липидов. Кинетика движения воды через роговой слой также снижается. Эти изменения, в дополнение к изменениям секреции кожного сала, вероятно, играют роль в распространенных заболеваниях кожи пожилых людей, особенно при ксерозе [2].
Эпидермис, самый поверхностный слой кожи, эволюционировал, чтобы сформировать барьер против окружающей среды. Он также обеспечивает поддержание гидратации. Этот многослойный эпителий включает несколько типов клеток: клетки Лангерганса, обеспечивающие иммунный надзор, меланоциты, обеспечивающие пигментацию кожи, клетки Меркеля, участвующие в механическом восприятии, и, наконец, кератиноциты, которые сами по себе составляют примерно 90% популяции эпидермиса и обеспечивают барьерную функцию. Для этого кератиноциты подвергаются постепенной дифференцировке вдоль вертикальной оси, ориентированной изнутри наружу. На терминальной стадии своей дифференцировки кератиноциты могут уподобляться мумифицированным клеткам, называемым корнеоцитами, лишенным ядра и клеточных органелл. Во время физиологического старения толщина эпидермиса значительно уменьшается, дермоэпидермальное соединение уплощается, а барьерная функция постепенно ухудшается с непосредственными последствиями повышенной восприимчивости к инфекциям и обезвоживанием, что усугубляется трансэпидермальной потерей воды. Истончение эпидермиса, связанное с дегенерацией барьерной функции, предполагает внутреннее изменение процесса дифференцировки кератиноцитов с возрастом. В отличие от других тканей хронологическое старение не влияет ни на количество, ни на функциональность эпидермальных стволовых клеток.
В отличие от эпидермиса, который состоит из соединенных и плотных клеток, дерма в основном состоит из внеклеточного матрикса (ВКМ). Коллагеновые волокна являются основным компонентом этой структуры. Они придают ему устойчивость к механическим ударам. Эластичные волокна, второй волокнистый элемент ВКМ, позволяют коже возвращаться к исходной форме после деформации. Наконец, протеогликаны и гликозаминогликаны (ГАГ) составляют гель, в котором закрепляются эти волокнистые компоненты и обеспечивают устойчивость к сжимающим силам. Этот гель также представляет собой самый большой запас воды в коже, в частности, благодаря очень высокой водоудерживающей способности одного из ГАГ, гиалуроновой кислоты. Все эти компоненты матрикса синтезируются и разрушаются резидентными клетками дермы, фибробластами. Эти клетки секретируют коллагеназы и протеазы, а также их ингибиторы для ремоделирования окружающего их ВКМ [3].
Процесс старения затрагивает каждый из компонентов дермы [4]. Действительно, в коже пожилых людей дезорганизована густая и прочная сеть коллагеновых волокон [3] в основном из-за нарушения баланса между синтезом и деградацией, возникающего в результате увеличения секреции коллагеназ ММП (матриксных металлопротеиназ) [5]. Основной причиной этого нарушения является увеличение АФК в стареющей коже, что может быть связано с митохондриальной дисфункцией в эпидермисе. Количество эластических волокон также уменьшается с физиологическим старением, что еще больше усиливает рыхлость сети дермального матрикса, вызывая появление морщин. Изменение этой фиброзной сети ведет параллельно к уменьшению взаимодействия фибробластов с ВКМ [4]. Эта потеря физического контакта клеток, связанная с многочисленными стрессами, которые они накапливают при физиологическом старении, такими как повреждение ДНК, окислительный стресс или даже воздействие ультрафиолетовых лучей (УФ), увеличивает количество клеток, вступающих в старение [6].
Старение и качество жизни
Старение кожи – это не просто проблема дряблости покровов. Скорее, это дефицит иммунитета, способы, которыми мы взаимодействуем и уравновешиваем микроорганизмы в нашей среде, как мы заживляем травматические раны, а также здоровье и благополучие тех самых стволовых клеток, поддерживающих орган, который является нашим основным интерфейсом с внешним миром. Более того, множество клеточных игроков и биологических путей служат не только парадигмой того, как факторы, внутренние и внешние по отношению к коже, взаимодействуют, вызывая патологический фенотип и дисфункцию старения, но и платформой, на которой мы можем понимать старение внекожных тканей.
Кроме того, снижение гидратации рогового слоя вовлечено в патогенез сенильного ксероза и зуда, связанного со старением [7, 8]. Предыдущие исследования показали, что снижение гидратации рогового слоя увеличивает воспалительную инфильтрацию, плотность тучных клеток, дегрануляцию тучных клеток и содержание гистамина в дерме мышей [9, 10]. Повышение уровня цитокинов и гистамина в коже может спровоцировать расчесывание из-за зуда, что приведет к нарушению барьера проницаемости эпидермиса, а это, в свою очередь, приведет к дальнейшему усилению кожного воспаления. Поскольку гомеостаз эпидермального барьера проницаемости в стареющей коже нарушен [11, 12], его нельзя быстро нормализовать, что приводит к устойчивому увеличению кожного воспаления и обострению ранее существовавших воспалительных состояний, таких как атопический дерматит и экзема. Более того, устойчивое увеличение кожного воспаления может в конечном итоге вызвать системное воспаление, что может привести к развитию заболеваний, связанных с воспалением [13, 14]. Кроме того, ночной зуд может вызывать бессонницу, приводящую к обострению других заболеваний, таких как сердечно-сосудистые заболевания и болезни Паркинсона [15, 16]. Таким образом, снижение гидратации рогового слоя может привести к развитию как кожных, так и внекожных нарушений.
Снижение содержания липидов в роговом слое может в значительной степени способствовать замедлению восстановления барьера проницаемости в стареющей коже [11, 12]. Соответственно, местное применение смеси липидов, содержащей три ключевых липида рогового слоя (холестерин, свободные жирные кислоты и церамиды), ускоряет восстановление барьера проницаемости как у старых мышей, так и у людей [17]. Недавнее исследование показало, что местное применение смягчающего средства, содержащего липиды рогового слоя, не только улучшает барьер проницаемости эпидермиса, гидратацию рогового слоя и рН поверхности кожи, но также снижает циркулирующие уровни провоспалительных цитокинов у пожилых людей [13]. Существует по крайней мере два возможных механизма, с помощью которых липидная смесь для местного применения улучшает функцию эпидермиса. Во-первых, топические липиды проникают в кератиноциты зернистого слоя, где они упаковываются в ламеллярные тельца, затем секретируются в роговой слой, где формируются ламеллярные бислои [18, 19]. Другой механизм заключается в том, что эта смесь липидов содержит жирные кислоты, которые могут активировать рецепторы, в свою очередь активируемые пролифератором пероксисом (PPAR) [20].
Возможности уходовых средств в уменьшении проявлений старения
С учетом возрастных изменений, происходящих в коже, пожилым пациентов вне зависимости от наличия зуда можно рекомендовать применение увлажняющих средств, которые позволят минимизировать последствия старения кожи. Одним из таких средств является увлажняющий крем LE SANTI c защитой от потери влаги. В его состав входят пантенол, биотический комплекс из пребиотиков и пробиотиков, натрия гиалуронат и натуральный комплекс гликоцерамидов, холестерина и фосфолипидов. Пантенол обладает регенерирующим и смягчающим действием, питает и быстро снимает раздражение, увеличивает прочность коллагеновых волокон. Натрия гиалуронат отвечает за глубокое увлажнение кожи, улучшает ее тонус и упругость. Но наибольший интерес представляет комплекс церамидов, восполняющий нехватку липидов и способствующий удержанию влаги в роговом слое. Как упоминалось ранее, липидные компоненты способны активировать рецепторы PPAR, которые играют роль в ослаблении воспалительных реакций и минимизации зуда, часто наблюдаемого у пожилых пациентов [21].
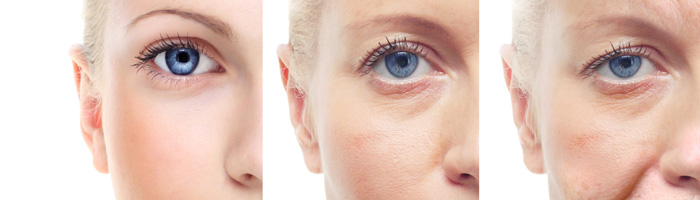
Наш опыт демонстрирует, что у возрастных пациентов с выраженным ксерозом нередко отмечается зуд (рис. 1).
Рисунок 1. Ксероз и зуд у возрастных пациентов

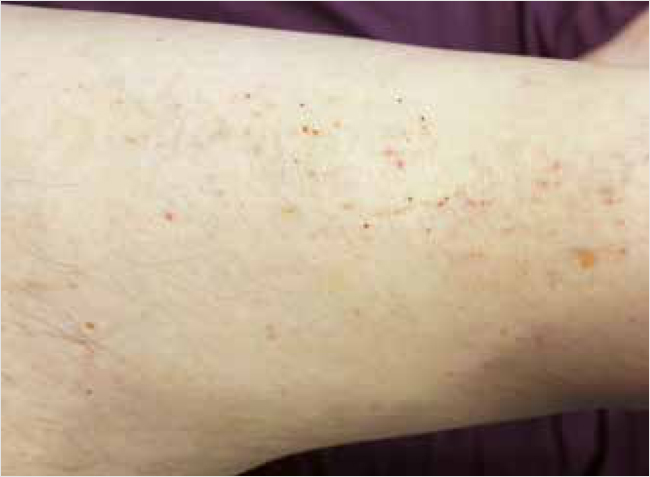
Применение увлажняющего крема LE SANTI позволяет уже к 7–10-му дню снять неприятные симптомы – зуд, чувство стянутости, шелушение (рис. 2).
Рисунок 2. Динамика кожных симптомов на 10-й день применения увлажняющего крема LE SANTI
Кроме того, длительное использование средства значимо изменяет краниометрические показатели кожи: увлажненность увеличивается почти в 1,5 раза и приближается к верхней границе нормальных возрастных показателей [22].
Заключение
Изменения, происходящие в коже с возрастом, влекут за собой снижение барьерной функции кожи, увеличение трансэпидермольной потери жидкости. Это, в свою очередь, проявляется ксерозом, зудом и другими симптомами, которые могут значительно снижать качество жизни данной возрастной группы. Применение средств ухода с выраженными увлажняющими и восстанавливающими свойствами позволяет избавить пациента от раздражающих проявлений старения кожи и минимизировать риски возникновения кожных заболеваний, связанных с нарушением проницаемости кожных покровов или их сниженной увлажненностью.
Список литературы / References
- Harvell J.D., Maibach H.I. Percutaneous absorption and inflammation in aged skin: a review. J Am Acad Dermatol. 1994;31(6):1015–1021. doi: 10.1016/S0190-9622(94)70273-X.
- Biniek K., Kaczvinsky J., Matts P., Dauskardt R.H. Understanding age-induced alterations to the biomechanical barrier function of human stratum corneum. J Dermatol Sci. 2015;80(2):94–101. doi: 10.1016/j.jdermsci.2015.07.016.
- Haydont V., Bernard B.A., Fortunel N.O. Age-related evolutions of the dermis: clinical signs, fibroblast and extracellular matrix dynamics. Mech Ageing Dev. 2019;177:150–156. doi: 10.1016/j.mad.2018.03.006.
- Shin J.W., Kwon S.H., Choi J.Y., Na J.I., Huh C.H., Choi H.R., Park K.C. Molecular mechanisms of dermal aging and antiaging approaches. Int J Mol Sci. 2019;20(9):2126. doi: 10.3390/ijms20092126.
- Lago J.C., Puzzi M.B. The effect of aging in primary human dermal fibroblasts. PLoS ONE. 2019;14(7):e0219165. doi: 10.1371/journal.pone.0219165.
- Gruber F., Kremslehner C., Eckhart L., Tschachler E. Cell aging and cellular senescence in skin aging – Recent advances in fibroblast and keratinocyte biology. Exp Gerontol. 2020;130:110780. doi: 10.1016/j.exger.2019.110780.
- Norman R.A. Xerosis and pruritus in the elderly: recognition and management. Dermatol Ther. 2003;16(3):254–259. doi: 10.1046/j.1529-8019.2003.01635.x.
- Valdes-Rodriguez R., Stull C., Yosipovitch G. Chronic pruritus in the elderly: pathophysiology, diagnosis and management. Drugs Aging. 2015;32(3):201–215. doi: 10.1007/s40266-015-0246-0.
- Ashida Y., Denda M. Dry environment increases mast cell number and histamine content in dermis in hairless mice. Br J Dermatol. 2003;149(2):240–247. doi: 10.1046/j.1365-2133.2003.05408.x.
- Denda M., Sato J., Tsuchiya T., Elias P.M., Feingold K.R. Low humidity stimulates epidermal DNA synthesis and amplifies the hyperproliferative response to barrier disruption: implication for seasonal exacerbations of inflammatory dermatoses. J Invest Dermatol. 1998;111(5):873–878. doi: 10.1046/j.1523-1747.1998.00364.x.
- Ghadially R., Brown B.E., Sequeira-Martin S.M., Feingold K.R., Elias P.M. The aged epidermal permeability barrier. Structural, functional, and lipid biochemical abnormalities in humans and a senescent murine model. J Clin Invest. 1995;95(5):2281–2290. doi: 10.1172/JCI117919.
- Ghadially R., Brown B.E., Hanley K., Reed J.T., Feingold K.R., Elias P.M. Decreased epidermal lipid synthesis accounts for altered barrier function in aged mice. J Invest Dermatol. 1996;106(5):1064–1069. doi: 10.1111/1523-1747.ep12338692.
- Ye L., Mauro T.M., Dang E., Wang G., Hu L.Z., Yu C. et al. Topical applications of an emollient reduce circulating pro-inflammatory cytokine levels in chronically aged humans: a pilot clinical study. J Eur Acad Dermatol Venereol. 2019;33(11):2197–2201. doi: 10.1111/jdv.15540.
- Hu L., Mauro T.M., Dang E., Man G., Zhang J., Lee D. et al. Epidermal Dysfunction Leads to an Age-Associated Increase in Levels of Serum Inflammatory Cytokines. J Invest Dermatol. 2017;137(6):1277–1285. doi: 10.1016/j.jid.2017.01.007.
- Bollu P.C., Sahota P. Sleep and Parkinson Disease. Mo Med. 2017;114(5):381–386. Available at: https://pubmed.ncbi.nlm.nih.gov/.
- Hepburn M., Bollu P.C., French B., Sahota P. Sleep Medicine: stroke and Sleep. Mo Med. 2018;115(6):527–532. Available at: https://pubmed.ncbi.nlm.nih.gov/.
- Denda M., Koyama J., Hori J., Horii I., Takahashi M., Hara M., Tagami H. Ageand sex-dependent change in stratum corneum sphingolipids. Arch Dermatol Res. 1993;285(7):415–417. doi: 10.1007/BF00372135.
- Man M.Q., Feingold K.R., Elias P.M. Exogenous lipids influence permeability barrier recovery in acetone-treated murine skin. Arch Dermatol. 1993;129(6):728–738. Available at: https://pubmed.ncbi.nlm.nih.gov/.
- Mao-Qiang M., Brown B.E., Wu-Pong S., Feingold K.R., Elias P.M. Exogenous nonphysiologic vs physiologic lipids. Divergent mechanisms for correction of permeability barrier dysfunction. Arch Dermatol. 1995;131(7):809–816. doi: 10.1001/archderm.131.7.809.
- Grygiel-Górniak B. Peroxisome proliferator-activated receptors and their ligands: nutritional and clinical implications – a review. Nutr J. 2014;13:17. doi: 10.1186/1475-2891-13-17.
- Sasso O., Summa M., Armirotti A., Pontis S., De Mei C., Piomelli D. The N-Acylethanolamine Acid Amidase Inhibitor ARN077 Suppresses Inflammation and Pruritus in a Mouse Model of Allergic Dermatitis. J Invest Dermatol. 2018;138(3):562–569. doi: 10.1016/j.jid.2017.07.853.
- Сакания Л.Р., Оленич И.В., Корсунская И. . Чувствительная кожа: что за этим стоит и как помочь пациентам? Медицинский алфавит. 2022;(8):75–78. doi: 10.33667/2078-5631-2022-8-75-78. / Sakaniya L.R., Olenich I.V., Korsunskaya I.M. Sensitive skin: What is behind it and how to help patients? Medical Alphabet. 2022;(8):75–78. (In Russ.) doi: 10.33667/2078-5631-2022-8-75-78.






