Журнал "Амбулаторная хирургия" № 2/2022
DOI: 10.21518/1995-1477-2022-19-2-142-151
А.Г. Хитарьян1,2, А.А. Абовян2*, А.В. Межунц1,2, А.А. Орехов1,2, Д.А. Мельников1,2, А.В. Саркисян2, С.А. Адизов1, А.А. Рогут1, Г.Д. Зиглер2, М.Ж.К. Амегнину2
1 Клиническая больница «РЖД-Медицина» г. Ростова-на-Дону»; 344011, Россия, Ростов-на-Дону, ул. Варфоломеева, д. 92а
2 Ростовский государственный медицинский университет; 344022, Россия, Ростов-на-Дону, пер. Нахичеванский, д. 29
Введение. Несмотря на большую популярность гастроеюношунтирования по Ру и продольной резекции желудка в лечении морбидного ожирения, недостаточно изученной остается проблема развития и прогрессирования признаков саркопении у больных с сахарным диабетом 2-го типа в послеоперационном периоде.
Цель. Изучить распространенность и динамику признаков саркопении у пациентов с сахарным диабетом 2-го типа после гастроеюношунтирования по Ру и лапароскопической продольной резекции желудка в отдаленные сроки.
Материалы и методы. Наше проспективное исследование включало 257 бариатрических пациентов (170 –гастроеюношунтирование по Ру и 87 – лапароскопическая продольная резекция желудка) с сахарным диабетом 2-го типа. Всем больным проводился стандартный комплекс дооперационного исследования с дополнительным определением индекса массы скелетной мускулатуры с помощью метода биоимпедансометрии. Через 6, 12, 18 и 24 мес. проводились контрольные обследования.
Результаты. На дооперационном этапе было выявлено 28 пациентов (16,5%) с признаками умеренной саркопении в группе гастроеюношунтирования по Ру и 15 пациентов (17,2%) в группе лапароскопической продольной резекции желудка. По данным биоимпедансометрии, через 24 мес. после операции в первой группе было выявлено 37 пациентов (25,9%) с признаками умеренной саркопении и 2 пациента (1,4%) с явлениями выраженной саркопении. Во второй группе через 24 мес. после операции статистической разницы по количеству пациентов с признаками саркопении в сравнении с дооперационным периодом не выявлено.
Выводы. Частота развития и прогрессирования признаков саркопении после гастроеюношунтирования по Ру статистически выше, чем после лапароскопической продольной резекции желудка. В связи с этим, по нашему мнению, при выборе метода оперативного лечения морбидного ожирения с сопутствующим сахарным диабетом 2-го типа необходима детальная оценка состояния белкового обмена методом биоимпедансометрии.
Для цитирования: Хитарьян А.Г., Абовян А.А., Межунц А.В., Орехов А.А., Мельников Д.А., Саркисян А.В., Адизов С.А., Рогут А.А., Зиглер Г.Д., Амегнину М. Риски развития саркопении после бариатрических операций у пациентов с сахарным диабетом 2-го типа. Амбулаторная хирургия. 2022;19(2):142-151. https://doi.org/10.21518/1995-1477-2022-19-2-142-151
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Risk of sarcopenia after bariatric surgery in patients with type 2 diabetes mellitus
Aleksandr G. Khitarian1,2, Arutyun A. Abovyan2*, Arut V. Mezhunts1,2, Aleksey A. Orekhov2, Denis A. Melnikov1, 2, Aram V. Sarkisyan2, Suleiman A. Adizov1, Alexander A. Rogut1, Gabriella J. Ziegler2, Carlos M.J. Amegninou2
1 Clinical Hospital Russian Railway-Medicine Rostov-on-Don; 92a, Varfolomeeva St., Rostov-on-Don, 344011, Russia
2 Rostov State Medical University, 29, Nakhichevansky Lane, Rostov-on-Don, 344022, Russia
Introduction. Despite the great popularity of Roux-en-Y gastric bypass and laparoscopic sleeve gastrectomy in the treatment of morbid obesity, the problem of the development and progression of sarcopenia in patients with type 2 diabetes mellitus in the postoperative period remains insufficiently studied.
Aim. To study the prevalence and dynamics of sarcopenia in patients with type 2 diabetes mellitus after Roux-en-Y gastric bypass and laparoscopic sleeve gastrectomy in the long term.
Materials and methods. Our prospective study included 257 bariatric patients (170 Roux-en-Y gastric bypass and 87 laparoscopic sleeve gastrectomy) with type 2 diabetes mellitus. All patients underwent a standard set of preoperative examination with obligatory determination of the skeletal muscle mass index using the bioelectrical impedance analysis. After 6, 12, 18 and 24 months, control examinations were carried out.
Results. At the preoperative stage, 28 patients (16.5%) with signs of moderate sarcopenia were identified in the Roux-en-Y gastric bypass group and 15 patients (17.2%) in the laparoscopic sleeve gastrectomy group. According to the bioelectrical impedance analysis, 24 months after the operation, 37 patients (25.9%) with signs of moderate sarcopenia and 2 patients (1.4%) with severe sarcopenia were identified in the first group. 24 months after surgery in the second group there was no statistical difference in the number of patients with signs of sarcopenia in comparison with the preoperative period.
Conclusion. The frequency of development and progression of signs of sarcopenia after Roux-en-Y gastric bypass is statistically higher than after laparoscopic sleeve gastrectomy. In this regard, in our opinion, when choosing a method of surgical treatment of morbid obesity with concomitant type 2 diabetes mellitus, a detailed assessment of the state of protein metabolism by the bioelectrical impedance analysis is necessary.
For citation: Khitaryan A.G., Abovyan A.A., Mezhunts A.V., Orekhov A.A., Melnikov D.A., Sarkisyan А.V., Adizov S.A., Rogut A.A., Ziegler G.J., Amegninou C.M. Risk of sarcopenia after bariatric surgery in patients with type 2 diabetes mellitus. Ambulatornaya khirurgiya = Ambulatory Surgery (Russia). 2022;19(2):142-151. (In Russ.) https://doi.org/10.21518/1995-1477-2022-19-2-142-151
Conflict of interest: the authors declare no conflict of interest.
Введение
На сегодняшний день лапароскопическая продольная резекция желудка (ЛПРЖ) и гастроеюношунтирование по Ру (РуГШ) являются одними из наиболее популярных бариатрических операций в мире [1]. Это связано с их достаточно высокой эффективностью в снижении веса и ремиссии сахарного диабета 2-го типа (СД2).
По данным P. Salminen, полная или частичная ремиссия СД2 наблюдалась у 37% пациентов после ЛПРЖ и у 45% после РуГШ [2]. Однако также известно, что пациенты с СД2 имеют более высокий риск развития саркопении по сравнению с пациентами с эугликемией [3, 4].
Сами по себе бариатрические вмешательства, особенно мальабсорбтивные, могут приводить к дефициту белков, витаминов и микроэлементов в организме, что требует медикаментозной коррекции. В ряде случаев выраженные нарушения мальабсорбции приводят к гипопротеинемии, уменьшению мышечной массы и саркопении [5–11]. Гипопротеинемия в послеоперационном периоде, по данным разных авторов, встречается не более чем у 6% бариатрических пациентов, при этом тяжелые случаи выявляются всего у 0,1% пациентов [12]. Вместе с тем оценка изменения мышечной массы до и после такого рода вмешательств, особенно у пациентов, страдающих СД2, является более тонким инструментом выявления белковой недостаточности, т. к. нарастание саркопении зачастую не сопровождается лабораторными проявлениями нарушения белкового обмена.
Диагностика саркопении имеет некоторые ограничения [13]. Методы визуализации с высоким разрешением, такие как магниторезонансная томография (МРТ) и компьютерная томография (КТ), рекомендованы Международной рабочей группой по саркопении как «золотой стандарт», однако они имеют высокую стоимость и сопровождаются радиационным облучением (КТ), поэтому оба метода не всегда доступны и целесообразны в клинических условиях. Несмотря на то что двухэнергетическая рентгеновская абсорбциометрия (ДЭРА) может считаться эталонным методом для измерения мышечной массы, она также непрактична для использования в крупных эпидемиологических исследованиях [13, 14]. По этой причине все больше исследований используют биоэлектрический импедансный анализ (биоимпедансометрия (БИМ)) для определения низкой мышечной массы в контексте саркопении [15–17]. Положительными сторонами этого метода являются низкая стоимость аппаратуры, отсутствие негативного воздействия на организм исследуемого при процедуре измерения, простота и доступность применения метода в лечебном учреждении или домашних условиях. Вероятно, поэтому БИМ — самый распространенный метод в публикациях, посвященных, в частности, метаболической хирургии [18].
Исследования по изучению мышечной массы тела пациентов, страдающих СД2, до и после бариатрических вмешательств немногочисленны. По данным C. Voican, при дооперационном обследовании пациентов саркопения была выявлена у 8%, а через год их количество возросло до 32% [19]. Также в 2020 г. была опубликована статья S. Heshka, в которой указывается более высокий расход энергии в покое через 5 лет у пациентов после РуГШ по сравнению с неоперированными исследуемыми с аналогичными антропометрическими показателями [20]. M. Pekař et al. указывают на снижение массы скелетной мускулатуры и минеральной массы костей по данным ДЭРА через 24 мес. после бариатрической операции [21].
Таким образом, на сегодняшний день чрезвычайно актуальным остается вопрос изучения развития саркопении после бариатрических операций. Следовательно, существует необходимость выделения групп риска по развитию саркопении в послеоперационном периоде и их учет при выборе метода операции.
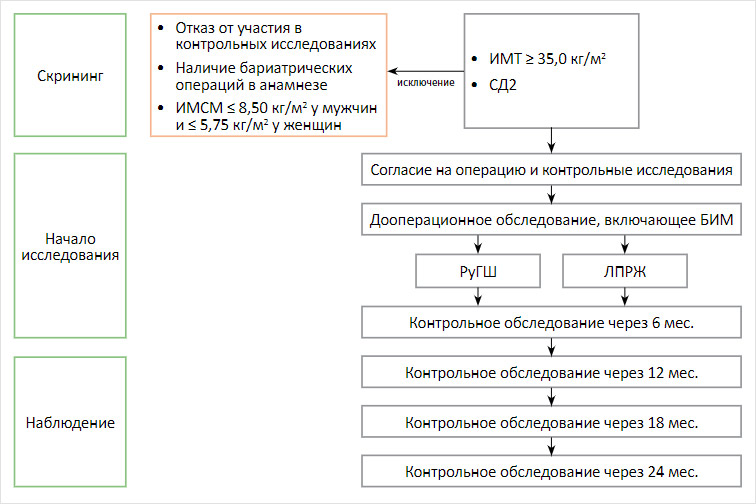
Целью нашего когортного проспективного исследования является изучение динамики прогрессирования признаков саркопении у бариатрических пациентов с CД2 после гастроеюношунтирования по Ру и лапароскопической продольной резекции желудка. Дизайн исследования представлен на рисунке.
Рисунок. Дизайн исследования
Материалы и методы
В данном проспективном исследовании нами были представлены результаты комплексного лечения 257 пациентов (200 женщин (77%), 57 мужчин (28%)) в возрасте от 22 до 76 лет, прооперированных по поводу морбидного ожирения, с установленным диагнозом СД (согласно критериям ВОЗ) (табл. 1). Исследование проводилось в ЧУЗ «КБ «РЖД-Медицина» г. Ростова-на-Дону с 2016 по 2020 г. В исследование были включены пациенты с периодом наблюдения не менее 2 лет (от 24 до 47 мес., медиана 38 мес.).
Таблица 1. Общая клиническая характеристика больных
| Показатель | Значение |
| Число больных | 257 |
| Женщины | 200 (78%) |
| Мужчины | 57 (22%) |
| Средний возраст (лет) | 46,4 ± 12,3 |
| Средняя масса тела (кг) | 132,2 ± 30,3 |
| Средний ИМТ (кг/м2) | 48,3 ± 10,8 |
| HbA1c (%) | 7,7 (6,5; 11,5) |
| Тип операции | |
| РуГШ | 170 (66%) |
| ЛПРЖ | 87 (34%) |
Критерии включения
– информированное добровольное согласие пациента на участие в исследовании, ИМТ > 35 кг/м2, наличие СД2, биоимпедансометрия (БИМ) до операции, наблюдение в течение не менее 18 мес. после операции.
Критерии исключения – отказ от участия в исследовании, наличие в анамнезе бариатрических операций, признаки тяжелой саркопении по данным БИМ.
Всем пациентам на дооперационном этапе выполнялся стандартный алгоритм обследования, указанный в клинических рекомендациях по бариатрической и метаболической хирургии, включающий антропометрию, исследование гликемических показателей (глюкоза крови, гликированный гемоглобин, инсулин, С-пептид), показателей белкового обмена (общий белок, альбумин), оценивалась липидограмма. Кроме того, с целью более детального изучения состояния белкового обмена всем исследуемым проводилась биоимпедансометрия (БИМ). Контрольные обследования проводились на 6, 12, 18 и 24 мес. после операции.
В соответствии с целью исследования все пациенты были разделены на две группы в зависимости от выполненного вмешательства: 170 пациентам выполнено РуГШ и 87 пациентам была выполнена ЛПРЖ. РуГШ выполнялось с формированием культи желудка на калибровочном зонде 36 Fr длиной 6–10 см и объемом менее 40 мл, наложением ручного гастроэнтероанастомоза. Длины билиарной и алиментарной петель составляли 100 и 150 см соответственно вне зависимости от ИМТ.
ЛПРЖ выполнялась на калибровочном зонде 36 Fr, резекция выполнялась от уровня 2 см проксимальнее пилорического жома до угла Гиса с обязательным укреплением линии степлерного шва серозно-мышечным швом нерассасывающимся, атравматичным шовным материалом.
БИМ проводилась на анализаторе обменных процессов и состава тела АВС-02 «МЕДАСС» (Россия) с соблюдением всех стандартных рекомендаций. Рекомендации по проведению процедуры БИМ включали следующие положения:
- последний прием пищи не ранее чем за два часа до исследования;
- исключение физических нагрузок за сутки до исследования;
- отказ от употребления алкоголя за сутки до исследования;
- процедура проводится лежа на спине на кушетке шириной не менее 80 см с отведенными правыми верхним и нижним конечностями;
- исключение контакта металлических предметов с телом исследуемого.
Нормальным индекс массы скелетной мускулатуры (ИМСМ) у мужчин считался при значении > 10,76 кг/м2. Диагноз умеренной саркопении устанавливался при ИМСМ = 8,51–10,75 кг/м2. ИМСМ < 8,51 кг/м2 указывает на тяжелую саркопению. У женщин в норме ИМСМ ≥ 6,76 кг/м2, умеренная – 5,76–6,75 кг/м2; тяжелая саркопения ≤ 5,75 кг/м2.
Статистический анализ
Сбор данных и формирование их в базу данных проводили с помощью электронных таблиц MS Excel 19.0 (Microsoft, США). Статистический анализ данных проводили при помощи программы Statistica SPSS 26.0 (IBM Statistic, США).
Количественные данные в первую очередь оценивались на предмет соответствия нормальному закону распределения с помощью критерия Шапиро – Уилка (при числе исследуемых менее 50) или критерия Колмогорова – Смирнова (при числе исследуемых более 50). Количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей (Q1 – Q3) ввиду отсутствия нормального распределения значений. Для сравнительного попарного анализа применяли непараметрический критерий U-Манна – Уитни. Различия между данными считаются статистически значимыми при р ≤ 0,05. И данные не имели статистически значимых различий, если р > 0,05.
При описании категориальных данных учитывали абсолютные значения (количество человек) и относительное значение (частоту встречаемости, процентное отношение, %).
Результаты
Исходные ИМТ в группах РуГШ и ЛПРЖ не имели статистических различий и составили 43,4 [39,2; 49,1] кг/м2 и 45,2 [41,6; 47,2] кг/м2 соответственно (р = 0,553). При контрольных исследованиях через 6, 12 и 18 мес. наблюдались удовлетворительные результаты снижения веса в обеих группах без статистических различий между группами (р > 0,5). Через 24 мес. после операции медианы ИМТ в указанных группах составили 29,1 [28; 30] кг/м2 и 29,6 [28; 30] кг/м2 (р = 0,044). Однако при оценке процента EWL при контрольных исследованиях между группами выявлены статистические различия. Так, на 6, 12, 18 и 24-й мес. данный показатель в группе ЛПРЖ составил 49 [47,1; 52], 65,2 [60,1; 69], 75,4 [71,2; 77] и 74 [68; 77] соответственно. В группе ЛПРЖ – 48,4 [47,2; 49,5], 62,8 [60; 67], 71,8 [70; 73] и 67,9 [66; 70].
Исследуемые группы не имели статистических различий по исходному уровню глюкозы и гликированного гемоглобина. Данные показатели в группе РуГШ составили 7,5 [7,2; 8,1] ммоль/л и 7,4% [7; 7,9] соответственно, а в группе ЛПРЖ — 7,6 [7,4; 7,9] и 7,5 [7,3; 7,8]. При контрольных исследованиях в обеих группах через 6, 12 и 18 мес. наблюдалось удовлетворительное снижение уровня глюкозы крови, статистических различий между группами не наблюдалось (p > 0,05). Через 24 мес. уровни глюкозы крови в группах РуГШ и ЛПРЖ имели статистические различия и составили 5,9 [5,6; 6,2] и 6,1 [5,9; 6,2] соответственно (p = 0,001). При анализе медиан уровней гликированного гемоглобина в исследуемых группах также отмечалась удовлетворительная положительная динамика в течение всего периода наблюдения, составив к 24-му мес. 5,9% [5,5; 6,1] в группе РуГШ и 5,9% [5,7; 6,1] в группе ЛПРЖ.
Динамика изменений липидного профиля в исследуемых группах была удовлетворительной в обеих группах исследуемых. Медиана уровня общего холестерина (ОХС) в группе РуГШ снизилась с 5,47 [4,3; 6,2] до 3,75 [3,3; 4] ммоль/л к 6-му мес. и 3,2 [2,9; 3,4] ммоль/л к 12-му мес. исследования. Затем на 18-м мес. исследования был зарегистрирован незначительный подъем медианы ОХС до 3,98 [3,8; 4,2], что, вероятно, связано с адаптацией организма к измененной анатомии и физиологии желудочно-кишечного тракта, а также расширением диеты. На 24-м мес. исследования вновь было отмечено снижение ОХС до 3,61 [3,1; 3,9] ммоль/л. В группе ЛПРЖ медиана дооперационного уровня ОХС составила 5,3 [4,5; 6,1] ммоль/л. На 6-м и 12-м мес. этот показатель составил 4,7 [3,6; 5,3] и 3,3 [2,6; 3,9] ммоль/л соответственно. На 18-м мес. медиана уровня ОХС в данной группе также показала незначительный рост до 4,3 [3,6; 4,9] ммоль/л, что, по нашему мнению, имеет одинаковые с группой РуГШ причины. На 24-м мес. исследования медиана ОХС составила 3,6 [3; 4,3] ммоль/л.
Исходные медианы уровней общего белка и альбумина в группе РуГШ были 72,5 [70; 78] г/л и 46 [42; 49] г/л соответственно. На 6, 12, 18 и 24-м мес. наблюдений уровень общего белка снизился до 70 [68; 74], 67 [66; 69] г/л, 66 [66; 67] г/л и 68 [67; 70] г/л соответственно, а уровень альбумина – до 42 [40; 45], 40 [39; 43], 39 [38; 42] и 40 [38; 43] г/л. В группе ЛПРЖ исходные медианы уровней общего белка и альбумина были 72 [68; 76] г/л и 47 [45; 49] г/л соответственно. На 6, 12, 18 и 24-м мес. наблюдений уровень общего белка снизился до 70 [67; 72], 68 [66; 71], 68 [67; 71,5] и 69 [68; 73] г/л соответственно, а уровень альбумина – до 45 [41; 47], 44 [41; 46], 43,5 [40,2; 45] и 44 [41; 46] г/л. За весь период наблюдения явления мальабсорбции не наблюдалось ни у одного пациента.
Динамика изменения антропометрических, гликемических показателей, а также липидного профиля и белкового обмена представлена в табл. 2.
Таблица 2. Динамика изменения антропометрических и гликемических показателей, а также липидного профиля и белкового обмена
Показатели | Группы | Период наблюдения | |||||||||||
Исх., n = 257 | 6 мес., n = 245 | 12 мес., n = 239 | 18 мес., n = 224 | 24 мес., n = 216 | |||||||||
| Антропометрические данные: | |||||||||||||
| Вес, кг | РуГШ | Me [Q1; Q3] | 118 [105; 137] | 91 [85; 101] | 84 [79; 91] | 79 [74; 81] | 80 [75; 82] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 125 [117; 134] | 94 [91; 100] | 86 [81; 89] | 80 [78; 82] | 83 [80; 84] | |||||||
| р | 0,049* | 0,027* | 0,121 | 0,001* | 0,001* | ||||||||
| ИМТ, кг/м2 | РуГШ | Me [Q1; Q3] | 43,4 [39,2; 49,1] | 33 [31; 36] | 30 [28,8; 32] | 28,9 [27,5; 29] | 29,1 [28; 30] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 45,2 [41,6; 47,2] | 33,9 [32; 35] | 30,6 [29; 31,5] | 28,7 [27; 29] | 29,6 [28; 30] | |||||||
| р | 0,553 | 0,688 | 0,448 | 0,522 | 0,044* | ||||||||
| % EWL | РуГШ | Me [Q1; Q3] | 49 [47,1; 52] | 65,2 [60,1; 69] | 75,4 [71,2; 77] | 74 [68; 77] | |||||||
| ЛПРЖ | Me [Q1; Q3] | 48,4 [47,2; 49,5] | 62,8 [60; 67] | 71,8 [70; 73] | 67,9 [66; 70] | ||||||||
| р | 0,001* | 0,029* | 0,0001* | 0,0001* | |||||||||
| Гликемические показатели: | |||||||||||||
| Глюкоза крови, ммоль/л | РуГШ | Me [Q1; Q3] | 7,5 [7,2; 8,1] | 6,5 [6,1; 6,8] | 6,3 [5,9; 6,6] | 6,1 [5,8; 6,3] | 5,9 [5,6; 6,2] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 7,6 [7,4; 7,9] | 6,4 [6,2; 6,9] | 6,2 [6,1; 6,5] | 6,1 [5,8; 6,2] | 6,1 [5,9; 6,2] | |||||||
| р | 0,227 | 0,889 | 0,537 | 0,543 | 0,001* | ||||||||
| HbA1С, % | РуГШ | Me [Q1; Q3] | 7,4 [7; 7,9] | 6,3 [5,9; 6,6] | 6,2 [5,8; 6,5] | 5,9 [5,6; 6,2] | 5,9 [5,5; 6,1] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 7,5 [7,3; 7,8] | 6,2 [6; 6,7] | 6,1 [6; 6,4] | 6 [5,7; 6,1] | 5,9 [5,7; 6,1] | |||||||
| р | 0,035 | 0,975 | 0,59 | 0,349 | 0,392 | ||||||||
| Инсулин, мкЕд/мл | РуГШ | Me [Q1; Q3] | 31,5 [27,6; 36,2] | 17 [14,9; 19] | 10,2 [9; 12,4] | 10,9 [9,7; 12,9] | 11,3 [9,8; 12,8] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 19,3 [17,2; 25,8] | 16,8 [13,9; 19,3] | 9,7 [8,4; 11,3] | 10,5 [9,3; 12,3] | 11,6 [10,3; 13,2] | |||||||
| р | 0,0001* | 0,55 | 0,029* | 0,32 | 0,197 | ||||||||
| С-пептид, нг/мл | РуГШ | Me [Q1; Q3] | 5,3 [4,7; 5,8] | 3 [2,6; 3,6] | 1,4 [1,26; 1,84] | 1,43 [1,2; 1,69] | 1,8 [1,5; 1,97] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 3,9 [3,5; 4,2] | 2,4 [2,1; 2,7] | 1,7 [1,52; 1,85] | 1,27 [1,1; 1,38] | 1,38 [1,25; 1,49] | |||||||
| р | 0,0001* | 0,0001* | 0,0001* | 0,0001* | 0,0001* | ||||||||
| Показатели липидного профиля: | |||||||||||||
| Общий ХС, ммоль/л | РуГШ | Me [Q1; Q3] | 5,47 [4,3; 6,2] | 3,75 [3,3; 4] | 3,2 [2,9; 3,4] | 3,98 [3,8; 4,2] | 3,61 [3,1; 3,9] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 5,3 [4,5; 6,1] | 4,7 [3,6; 5,3] | 3,3 [2,6; 3,9] | 4,3 [3,6; 4,9] | 3,6 [3; 4,3] | |||||||
| р | 0,863 | 0,0001* | 0,364 | 0,001* | 0,18 | ||||||||
| ХС-ЛПНП, ммоль/л | РуГШ | Me [Q1; Q3] | 3,3 [2,9; 3,4] | 2,5 [2,3; 2,78] | 2,28[2,16; 2,5] | 1,9 [1,7; 2,2] | 1,92 [1,8; 2,2] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 3,2 [2,54; 3,3] | 3,1 [2,5; 3,19] | 2,46 [2; 2,73] | 2,25 [1,7; 2,5] | 1,96 [1,5; 2,17] | |||||||
| р | 0,018* | 0,0001* | 0,015* | 0,0001* | 0,19 | ||||||||
| ХС-ЛПОНП, ммоль/л | РуГШ | Me [Q1; Q3] | 0,93 [0,8; 0,99] | 0,72 [0,63; 0,81] | 0,42 [0,4; 0,51] | 0,6 [0,57; 0,72] | 0,52 [0,48; 0,63] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 0,9 [0,8; 0,98] | 0,81 [0,73; 0,9] | 0,45 [0,3; 0,54] | 0,75 [0,7; 0,84] | 0,5 [0,43; 0,6] | |||||||
| р | 0,371 | 0,0001* | 0,742 | 0,0001* | 0,087 | ||||||||
| ХС-ЛПВП, ммоль/л | РуГШ | Me [Q1; Q3] | 1,4 [1,17; 1,64] | 1 [0,95; 1,18] | 0,99 [0,9; 1,13] | 1,2 [1,15; 1,38] | 1 [0,96; 1,2] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 1,23 [1; 1,34] | 1,13 [0,98; 1,24] | 1 [0,86; 1,07] | 1,3 [1,2; 1,39] | 1 [0,92; 1,18] | |||||||
| р | 0,0001* | 0,131 | 0,45 | 0,032* | 0,314 | ||||||||
| Триглицериды, ммоль/л | РуГШ | Me [Q1; Q3] | 1,49 [1,39; 1,72] | 1,32 [1,23; 1,55] | 0,9 [0,79; 1,13] | 0,95 [0,87; 1] | 1,13 [1; 1,27] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 1,97 [1,49; 2,35] | 1,51 [1; 1,83] | 0,89 [0,7; 1,13] | 0,9 [0,76; 1,23] | 1 [0,95; 1,36] | |||||||
| р | 0,0001* | 0,388 | 0,223 | 0,217 | 0,238 | ||||||||
| Показатели белкового обмена: | |||||||||||||
| Общий белок, г/л | РуГШ | Me [Q1; Q3] | 72,5 [70; 78] | 70 [68; 74] | 67 [66; 69] | 66 [66; 67] | 68 [67; 70] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 72 [68; 76] | 70 [67; 72] | 68 [66; 71] | 68 [67; 71,5] | 69 [68; 73] | |||||||
| р | 0,024* | 0,008* | 0,017* | 0,0001* | 0,0001* | ||||||||
| Альбумин, г/л | РуГШ | Me [Q1; Q3] | 46 [42; 49] | 42 [40; 45] | 40 [39; 43] | 39 [38; 42] | 40 [38; 43] | ||||||
| ЛПРЖ | Me [Q1; Q3] | 47 [45; 49] | 45 [41; 47] | 44 [41; 46] | 43,5 [40,2; 45] | 44 [41; 46] | |||||||
| р | 0,187 | 0,0001* | 0,0001* | 0,0001* | 0,0001* | ||||||||
* Различия статистически значимы при р < 0,05.
В группе РуГШ (n = 170) исходно нормальный индекс массы скелетной мускулатуры (ИМСМ) имели 142 (83,5%) исследуемых (113 женщин и 29 мужчин), умеренная саркопения отмечалась у 28 (16,5%) исследуемых (22 женщины и 6 мужчин). Через 24 мес. после операции (n = 143) нормальный ИМСМ сохранялся у 104 (72,7%) исследуемых (82 женщины и 22 мужчины), умеренная саркопения была выявлена у 37 (25,9%) исследуемых (29 женщин и 8 мужчин), а выраженная – у 2 исследуемых женщин (1,4%).
В группе ЛПРЖ (n = 87) дооперационный нормальный ИМСМ имели 72 (82,8%) исследуемых (53 женщины и 19 мужчин), умеренная саркопения отмечалась у 15 (17,2%) исследуемых (12 женщин и 3 мужчины). На 24-й мес. (n = 73) нормальный ИМСМ сохранялся у 58 (79,5%) исследуемых (42 женщины и 16 мужчин), умеренная саркопения — у 15 (20,5%) исследуемых (12 женщин и 3 мужчины). В данной группе признаков выраженной саркопении не отмечалось ни в одном наблюдении.
Результаты изменения ИМСМ по данным БИМ в группах больных представлены в табл. 3.
Таблица 3. Частота развития саркопении
РуГШ: | |||||
| Степень саркопении | Период наблюдения | ||||
Исх., n = 170 | 24 мес., n = 143 | ||||
| норма | М > 10,76 кг/м2 | 29 | ∑142(83,5%) | 22 | ∑104(72,7%) |
| Ж ≥ 6,76 кг/м2 | 113 | 82 | |||
| умеренная | М 8,51–10,75 кг/м2 | 6 | ∑28(16,5%) | 8 | ∑37(25,9%) |
| Ж 5,76–6,75 кг/м2 | 22 | 29 | |||
| выраженная | М ≤ 8,5 кг/м2 | 0 | - | 0 | ∑2(1,4%) |
| Ж ≤ 5,75 кг/м2 | 0 | 2 | |||
ЛПРЖ: | |||||
| Степень саркопении | Период наблюдения | ||||
| Исх., n = 87 | 24 мес., n = 73 | ||||
| норма | М > 10,76 кг/м2 | 19 | ∑72(82,8%) | 16 | ∑58(79,5%) |
| Ж ≥ 6,76 кг/м2 | 53 | 42 | |||
| умеренная | М 8,51–10,75 кг/м2 | 3 | ∑15(17,2%) | 3 | ∑15(20,5%) |
| Ж 5,76–6,75 кг/м2 | 12 | 12 | |||
| выраженная | М ≤ 8,5 кг/м2 | 0 | - | 0 | - |
| Ж ≤ 5,75 кг/м2 | 0 | 0 | |||
Примечание. Согласно критерию χ2-Пирсона в группе РуГШ между периодом наблюдения (исходный/24 мес.) в зависимости от степени саркопении имеются статистически значимые различия (р = 0,033). В группе ЛПРЖ согласно критерию χ2-Пирсона между периодом наблюдения (исходный/24 мес.) в зависимости от степени саркопении не имеется статистически значимых различий (р = 0,59).
Обсуждение
В статье, опубликованной M. Patti, сделан вывод о том, что современные нехирургические методы лечения неэффективны для обеспечения устойчивого снижения веса [22]. Из различных вариантов лечения бариатрическая хирургия остается наиболее эффективным методом достижения долгосрочной потери веса [23, 24]. По данным нашего исследования отмечалось снижение медианы ИМТ в группе РуГШ с 43,4 [39,2; 49,1] до 29,1 [28; 30] кг/м2 в течение 24 мес. (медиана процента EWL составила 74 [68; 77]). В группе ЛПРЖ – с 45,2 [41,6; 47,2] до 29,6 [28; 30] кг/м2 (средний процент EWL составил 67,9 [66; 70]). Согласно литературным данным, послеоперационная потеря веса улучшает все сопутствующие ожирению заболевания, качество жизни и снижает общую смертность [25–27]. Также имеются данные, что у пациентов после бариатрических хирургических вмешательств наблюдается снижение заболеваемости диабетом на 83%, инфарктов миокарда и инсультов на 30–40%, снижение заболеваемости раком у женщин на 42% и общей смертности на 30–40% [22].
Сравнивая ЛПРЖ и РуГШ, P. Schauer et al. отмечают лучшие результаты гликемического контроля во второй группе. Сроки наблюдения в этом исследовании составили 12 мес. [28]. L. Qi et al. в своем метаанализе, опубликованном в 2017 г., также отметили, что РуГШ имело более высокую эффективность в сравнении с другими бариатрическими вмешательствами [29]. По данным систематического обзора, опубликованного H. Borgeraas в 2020 г., частота ремиссии СД2 через 1 год также была выше среди тех, кому было выполнено РуГШ, по сравнению с теми, кто подвергался ЛПРЖ [30]. В нашем исследовании также наблюдался удовлетворительный контроль гликемических показателей в течение 24 мес. после операции. Так, в группе РуГШ медиана уровня глюкозы крови снизилась с 7,5 [7,2; 8,1] до 5,9 [5,6; 6,2] ммоль/л через 24 мес., а средний уровень гликированного гемоглобина – с 7,4% [7; 7,9] до 5,9% [5,5; 6,1]. В группе ЛПРЖ медианы показателей глюкозы и гликированного гемоглобина снизились с 7,6 [7,4; 7,9] до 6,1 [5,9; 6,2] ммоль/л и с 7,5% [7,3; 7,8] до 5,9% [5,7; 6,1] соответственно.
Несомненно, бариатрическая хирургия по сравнению с консервативными методами обеспечивает быстрое и устойчивое снижение веса [31–34]. Хотя этот эффект преимущественно основан на желаемом снижении жировой массы, он также может быть связан с уменьшением других тканей, таких как мышечная и костная [35]. Ряд авторов сообщает, что после бариатрической операции у пациентов с СД2 мышечная сила и функция снижены по сравнению с контрольной группой [36, 37]. По результатам нашего исследования в группе РуГШ через 24 мес. после операции было выявлено 25,9% случаев умеренной саркопении против 16,5% на дооперационном этапе. Кроме того, было выявлено 1,4% (2 пациента) с выраженной саркопенией. В группе ЛПРЖ — 20,5% против 17,2% на дооперационном этапе. Различия между периодами наблюдения в данной группе статистически незначимы (р = 0,59).
Известно, что и ожирение, и саркопения увеличивают риски для здоровья, особенно когда речь идет об их сочетании, поэтому Европейское общество клинического питания и метаболизма (ESPEN) и Европейская ассоциация по изучению ожирения (EASO) призывают исследователей и клиницистов изучить и бороться с саркопеническим ожирением [38].
На сегодняшний день для оценки состояния белкового обмена принято ориентироваться на результаты лабораторных анализов крови (общий белок и альбумин), однако зачастую это оказывается недостаточно чувствительным методом диагностики. В свою очередь, нарастание признаков саркопении может указывать на серьезные нарушения белкового обмена. Так, наряду с хорошими результатами в стойком снижении веса, контроле гликемии, липидного профиля, а также удовлетворительными показателями белкового обмена на протяжении всего периода исследования, нами были выявлены пациенты с умеренной и выраженной саркопенией по данным БИМ. Следует отметить, что в группе РуГШ прогрессирование признаков саркопении было более выражено по сравнению с группой ЛПРЖ, что может объясняться наличием мальабсорбтивного компонента операции. Таким образом, при выборе метода оперативного лечения морбидного ожирения у пациентов с СД2, осложненным саркопенией, следует отказаться от мальабсорбтивных вмешательств.
Выводы
Морбидное ожирение, ассоциированное с СД2, нередко сочетается с явлениями саркопении (16,7% по данным нашего исследования).
По данным БИМ, через 24 мес. после РуГШ частота встречаемости умеренной саркопении составила 25,9% против 16,5% в дооперационном периоде. Частота выраженной саркопении – 1,4%. В группе ЛПРЖ статистической разности между периодами наблюдения не выявлено.
Учитывая достоверную зависимость частоты развития саркопении от выбранного метода операции, по нашему мнению, необходима детальная оценка состояния белкового обмена в предоперационном периоде с целью выбора более безопасной хирургической тактики.
Список литературы / References
- Reoch J., Motillo S., Shimony A., Filion K.B., Christou N.V., Joseph L. et al. Safety of laparoscopic vs open bariatric surgery: a systematic review and meta-analysis. Arch Surg. 2011;146:1314-1322. https://doi.org/10.1001/archsurg.2011.270.
- Salminen P., Helmiö M., Ovaska J., Juuti A., Leivonen M., Peromaa-Haavisto P. et al. Effect of Laparoscopic Sleeve Gastrectomy vs Laparoscopic Roux-en-Y Gastric Bypass on Weight Loss at 5 Years Among Patients With Morbid Obesity: The SLEEVEPASS Randomized Clinical Trial. JAMA. 2018;319(3):241-254. https://doi.org/10.1001/jama.2017.20313.
- Anagnostis P., Gkekas N.K., Achilla C., Pananastasiou G., Taouxidou P., Mitsiou M. et al. Type 2 Diabetes Mellitus is Associated with Increased Risk of Sarcopenia: A Systematic Review and Meta-analysis. Calcif Tissue Int. 2020;107:453-463. https://doi.org/10.1007/s00223-020-00742-y.
- Sarodnik C., Bours S.P.G., Schaper N.C., van den Bergh J.P., van Geel T.A.C.M. The risks of sarcopenia, falls and fractures in patients with type 2 diabetes mellitus. Maturitas. 2018;109:70-77. https://doi.org/10.1016/j.maturitas.2017.12.011.
- Xanthakos S.A. Nutritional deficiencies in obesity and after bariatric surgery. Pediatr Clin North Am. 2009;56:1105-1121. https://doi.org/10.1016/j.pcl.2009.07.002.
- Kaidar-Person O., Person B., Szomstein S., Rosenthal R.J. Nutritional deficiencies in morbidly obese Patients: a new form of Malnutrition? Obes Surg. 2008;18:870-876. https://doi.org/10.1007/s11695-007-9349-y.
- Stein J., Stier C., Raab H., Weiner R. Review article: the nutritional and pharmacological consequences of obesity surgery. Aliment Pharmacol Ther. 2014;40:582-609. https://doi.org/10.1111/apt.12872.
- Parrott J., Frank L., Rabena R., Craggs-Dino L., Isom K.A., Greiman L. American society for metabolic and bariatric surgery integrated health nutritional guidelines for the surgical weight loss patient 2016 Update: micronutrients. Surg Obes Relat Dis. 2017;13(5):727-741. https://doi.org/10.1016/j.soard.2016.12.018.
- Chaston T.B., Dixon J.B., O’Brien P.E. Changes in fat-free mass during significant weight loss: a systematic review. Int J Obes. 2007;31:743-750. https://doi.org/10.1038/sj.ijo.0803483.
- Strain G.W., Gagner M., Pomp A., Dakin G., Inabnet W.B., Hsieh J. et al. Comparison of weight loss and body composition changes with four surgical procedures. Surg Obes Relat Dis. 2009;5(5):582-587. https://doi.org/10.1016/j.soard.2009.04.001.
- Strain G.W., Gagner M., Pomp A., Dakin G., Inabnet W.B., Saif T. Comparison of fat-free mass in super obesity (BMI≥50 kg/m2) and morbid obesity (BMI<50 kg/m2) in response to different weight loss surgeries. Surg Obes Relat Dis. 2012;8:255-259. https://doi.org/10.1016/j.soard.2011.09.028.
- Fieber J.H., Sharoky C.E., Wirtalla C., Williams N.N., Dempsey D.T., Kelz R.R. The Malnourished Patient With Obesity: A Unique Paradox in Bariatric Surgery. J Surg Res. 2018;232:456-463. https://doi.org/10.1016/j.jss.2018.06.056.
- Sanz-Requena R., Martínez-Arnau F.M., Pablos-Monzó A., Flor-Rufino C., Barrachina-Igual J., García-Martí G. et al. The Role of Imaging Biomarkers in the Assessment of Sarcopenia. Diagnostics (Basel). 2020;10(8):534. https://doi.org/10.3390/diagnostics10080534.
- Buckinx F., Landi F., Cesari M., Fielding R.A., Visser M., Engelke K. et al. Pitfalls in the measurement of muscle mass: a need for a reference standard. J Cachexia Sarcopenia Muscle 2018;9(2):269-278. https://doi.org/10.1002/jcsm.12268.
- Graf C.E., Pichard C., Herrmann F.R., Sieber C.C., Zekry D., Genton L. Prevalence of low muscle mass according to body mass index in older adults. Nutrition. 2017;34:124-129. https://doi.org/10.1016/j.nut.2016.10.002.
- Lardiés-Sánchez B., Sanz-Paris A., Boj-Carceller D., Cruz-Jentoft A.J. Systematic review: prevalence of sarcopenia in ageing people using bioelectrical impedance analysis to assess muscle mass. Eur Geriatr Med. 2016;7(3):256-261. https://doi.org/10.1016/j.eurger.2016.01.014.
- Shafiee G., Keshtkar A., Soltani A., Ahadi Z., Larijani B., Heshmat R. Prevalence of sarcopenia in the world: a systematic review and meta-analysis of general population studies. J Diabetes Metab Disord. 2017;16:21. https://doi.org/10.1186/s40200-017-0302-x.
- Dixon J.B., Bhasker A.G., Lambert G.W., Lakdawala M. Leg to leg bioelectrical impedance analysis of percentage fat mass in obese patients-Can it tell us more than we already know? Surg Obes Relat Dis. 2016;12:1397-1402. https://doi.org/10.1016/j.soard.2016.01.027.
- Voican C.S., Lebrun A., Maitre S., Lainas P., Lamouri K., Njike-Nakseu M. et al. Predictive score of sarcopenia occurrence one year after bariatric surgery in severely obese patients. PLoS ONE. 2018;13(5):e0197248. https://doi.org/10.1371/journal.pone.0197248.
- Heshka S., Lemos T., Astbury N.M., Widen E., Davidson L., Goodpaster B.H. Resting Energy Expenditure and Organ-Tissue Body Composition 5 Years After Bariatric Surgery. Obes Surg. 2020;30:587-594. https://doi.org/10.1007/s11695-019-04217-4.
- Pekař M., Pekařová A., Bužga M., Holéczy P., Soltes M. The risk of sarcopenia 24 months after bariatric surgery -assessment by dual energy X-ray absorptiometry (DEXA): a prospective study. Videosurgery Miniinv. 2020;15:583-587. https://doi.org/10.5114/wiitm.2020.93463.
- Patti M.E., Goldfine A.B. Hypoglycemia after gastric bypass: the dark side of GLP-1. Gastroenterology. 2014;146:605-608. https://doi.org/10.1053/j.gastro.2014.01.038.
- Sjöström L., Lindroos A.K., Peltonen M., Torgerson J., Bouchard C., Carlsson B. et al. Lifestyle, diabetes, and cardiovascular risk factors 10 years after bariatric surgery. N Engl J Med. 2004;351:2683-2693. https://doi.org/10.1056/NEJMoa035622.
- Sjostrom L., Narbro K., Sjöström C.D., Karason K., Larsson B., Wedel H., et al. Effects of bariatric surgery on mortality in Swedish obese subjects. N Engl J Med. 2007;357(8):741-752. https://doi.org/10.1056/NEJMoa066254.
- Ford K.R., Khoury J.C., Biro F.M. Early markers of pubertal onset: height and foot size. J Adolesc Health. 2009;44:500-501. https://doi.org/10.1016/j.jadohealth.2008.10.004.
- Herpertz S., Kielmann R., Wolf A.M., Langkafel M., Senf W., Hebebrand J. Does obesity surgery improve psychosocial functioning? A systematic review. Int J Obes Relat Metab Disord. 2003;27:1300-1314. https://doi.org/10.1038/sj.ijo.0802410.
- McTigue K.M., Harris R., Hemphill B., Lux L., Sutton S., Bunton A. et al. Screening and interventions for obesity in adults: summary of the evidence for the U.S. Preventive Services Task Force. Ann Intern Med. 2003;139:933-949. https://doi.org/10.7326/0003-4819-139-11200312020-00013.
- Schauer P.R., Bhatt D.L., Kirwan J.P., Wolski K., Brethauer S.A., Navaneethan S.D. et al. Bariatric surgery versus intensive medical therapy for diabetes: 3-year outcomes. N Engl J Med 2014;370:2002-2013. https://doi.org/10.1056/NEJMoa1401329.
- Qi L., Guo Y., Liu C.-Q., Huang Z-P., Sheng Y., Zou D.-J. Effects of bariatric surgery on glycemic and lipid metabolism, surgical complication and quality of life in adolescents with obesity: a systematic review and meta-analysis. Surg Obes Relat Dis. 2017;13(12):2037-2055. https://doi.org/10.1016/j.soard.2017.09.516.
- Borgeraas H., Hofsø D., Hertel J.K., Hjelmesaeth J. Comparison of the effect of Roux-en-Y gastric bypass and sleeve gastrectomy on remission of type 2 diabetes: A systematic review and meta-analysis of randomized controlled trials. Obes Rev. 2020;21:e13011. https://doi.org/10.1111/obr.13011.
- Adamczyk P., Buzga M., Holeczy P., Švagera Z., Zonča P., Sievänen H., Pluskiewicz W. Body size, bone mineral density and body composition in obese women after laparoscopic sleeve gastrectomy: a 1-year longitudinal study. Horm Metab Res. 2015;47:873-879. https://doi.org/10.1055/s-0035-1555758.
- Bužga M., Marešová P., Petřeková K., Holéczy P., Kuča K. The efficacy of selected bariatric surgery methods on lipid and glucose metabolism: a retrospective 12-month study. Cent Eur J Public Health. 2018;26:49-53. https://doi.org/10.21101/cejph.a4637.
- Kasalický M., Bařinka A., Čierny M., Fried M., Gryga A., Holéczy P. et al. 10 years of sleeve gastrectomy in the Czech Republic in terms of the surgical procedure. Rozhl Chir. 2016;95:425-431. Available at: https://www.prolekare.cz/en/journals/perspectives-insurgery/2016-12-1/10-years-of-sleeve-gastrectomy-in-the-czech-republic-in-terms-of-the-surgical-procedure-60220.
- Bužga M., Hauptman K., Švagera Z., Hauptman K., Holéczy P. Metabolic effects of sleeve gastrectomy andl aparoscopic greater curvature plication: an 18-month prospective, observational, open-label study. Obes Surg. 2017;27:3258-3266. https://doi.org/10.1007/s11695-017-2779-2.
- Adamczyk P., Bužga M., Holéczy P., Švagera Z., Šmajstrla V., Zonča P., Pluskiewicz W. Bone mineral density and body composition afterl aparoscopic sleeve gastrectomy in men: a short-terml ongitudinal study. Int J Surg. 2015;23:101-107. https://doi.org/10.1016/j.ijsu.2015.09.048.
- Park S.W., Goodpaster B.H., Strotmeyer E.S., de Rekeneire N., Harris T.B., Schwartz A.V. et al. Decreased muscle strength and quality in older adults with type 2 diabetes: the health, aging, and body composition study. Diabetes. 2006;55(6):1813-1818. https://doi.org/10.2337/db05-1183.
- Park S.W., Goodpaster B.H., Strotmeyer E.S., Kuller L.H., Broudeau R., Kammerer C. et al. Health, Aging, and Body Composition Study. Accelerated loss of skeletal muscle strength in older adults with type 2 diabetes: the health, aging, and body composition study. Diabetes Care. 2007;30:1507-1512. https://doi.org/10.2337/dc06-2537.
- Barazzoni R., Bischoff S., Boirie Y., Busetto L., Cederholm T., Dicker D. et al. Sarcopenic obesity: time to meet the challenge. Obes Facts. 2018;11(4):294-305. https://doi.org/10.1159/000490361.
