
Журнал "Медицинский совет" №4/2023
DOI: 10.21518/ms2023-016
Р.А. Бонцевич1,2*, В.К. Котлярова1, А.В. Губарев1, О.А. Букач1, Д.Г. Дубоносова1,3, И.Г. Ростовцева1,3
1 Белгородский государственный национальный исследовательский университет; 308015, Россия, Белгород, ул. Победы, д. 85
2 Медицинский центр «Азбука здоровья»; 308024, Россия, Белгород, ул. Щорса, д. 37А
3 Городская поликлиника города Белгорода; 308600, Россия, Белгород, Белгородский пр-т, 99
Введение. Вопросы рационального лечения новой коронавирусной инфекции (НКИ), соответствия врачебных назначений клиническим рекомендациям с начала пандемии являются крайне актуальными. Особо важной представляется проблема избыточного назначения антимикробных препаратов.
Цель. Провести анализ назначений лекарственных средств (ЛС) и оценить результаты внедрения программы поддержки принятия врачебных решений (ПППР) среди врачей-терапевтов и врачей общей практики амбулаторного звена г. Белгорода при лечении НКИ.
Материалы и методы. Изучались схемы терапии пациентов амбулаторного звена с подтвержденной или вероятной инфекцией COVID-19. Исследование проведено в два этапа: до и после внедрения ПППР. В основной группе (ОГ, отделения поликлиники г. Белгорода с внедренной ПППР) проанализировано 95 эпизодов лечения до внедрения ПППР и 94 – после. В контрольной группе (КГ, без внедрения ПППР) – по 48 эпизодов на 1-м и 2-м этапе. Оценены назначения основных групп ЛС, их соответствие рекомендациям, оценено влияние внедрения ПППР на применяемые схемы терапии. Статистический анализ проводился с использованием четырехпольных и многопольных таблиц сопряженности с использованием критерия χ2 Пирсона, точного критерия Фишера.
Результаты. Проанализировано 285 схем терапии НКИ. В ходе исследования определена структура назначений ЛС. Установлено, что на фоне внедрения ПППР специалисты ОГ статистически значимо уменьшили необоснованное назначение антибактериальных препаратов (с 24,2 до 6,4%, p < 0,001; в КГ – р > 0,05; p(ОГ-КГ) < 0,001), реже назначали антикоагулянты (p(ОГ-КГ) > 0,05); значимо реже – системные глюкокортикоиды (p(ОГ-КГ) < 0,001), группу муколитических, бронхолитических и противокашлевых ЛС (p(ОГ-КГ) < 0,01), витамины (p(ОГ-КГ) < 0,001); значимо чаще (p(ОГ-КГ) < 0,05) – местные антисептики и группу прочих ЛС. Не выявлено значимых различий (p(ОГ-КГ) > 0,05) на 2-м этапе исследования в применении противовирусных, иммуномодулирующих, нестероидных противовоспалительных средств.
Заключение. В ходе исследования была определена структура назначений и выявлен ряд нерациональных терапевтических предпочтений среди врачей амбулаторного звена, касающихся лечения НКИ. Мы предполагаем, что дальнейшие врачебные образовательные мероприятия, совершенствование и рациональное использование ПППР помогут улучшить качество ведения пациентов с НКИ.
Для цитирования: Бонцевич Р.А., Котлярова В.К., Букач О.А., Губарев А.В., Дубоносова Д.Г., Ростовцева И.Г. Анализ подходов к лечению и эффективность применения программы поддержки принятия решений в поликлинической практике в период ковид-пандемии. Медицинский Совет. 2023;(4):77-85. https://doi.org/10.21518/ms2023-016
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Analysis of treatment approaches and the efficiency of application of a decision support program in polyclinic practice during the covid-pandemic period
Roman A. Bontsevich1,2*, Victoria K. Kotlyarova1, Artem V. Gubarev1, Olesya A. Bukach1, Diana G. Dubonosova1,3, Irina G. Rostovceva1,3
1 Belgorod State National Research University; 85, Pobedy St., Belgorod, 308015, Russia
2 Medical Center “Azbuka Zdorovya”, 37А, Shchors St., Belgorod, 308024, Russia
3 Belgorod City Polyclinic; 99, Belgorodsky Ave., Belgorod, 308600, Russia
Introduction. The issues of rational treatment of a new coronavirus infection (NCI), compliance of medical prescriptions with current clinical recommendations have been extremely relevant since the beginning of the pandemic. Of particular importance is the problem of overprescribing antimicrobials.
Aim. To analyze the prescriptions of medicines and evaluate the results of the implementation of the medical decision support system (MDSS) among general practitioners and general practitioners of the Belgorod outpatient department in the treatment of NCI.
Materials and methods. Treatment regimens for outpatient patients with confirmed or probable COVID-19 infection were studied. The study was carried out in two stages: before and after the implementation of the MDSS: in the main group (MG, departments of the Belgorod polyclinic with the implemented MDSS), 95 episodes of treatment were analyzed before the implementation of the MDSS and 94 after. In the control group (CG, without the introduction of MDSS) – 48 episodes at the 1st and 2nd stages. The prescriptions of the main groups of drugs, their compliance with the recommendations were assessed, the impact of the introduction of MDSS on the applied therapy regimens was assessed. Statistical analysis was performed using four-field and multi-field contingency tables using Pearson’s χ2 test, Fisher’s exact test.
Results. The 285 NCI therapy regimens were analyzed. In the course of the study, the structure of drug prescriptions was determined. It was found that against the background of the implementation of the MDSS, the specialists of the MG statistically significantly reduced the unreasonable prescription of antibacterial drugs (from 24.2 to 6.4%, p < 0.001; in the CG, p > 0.05; p(MG-CG) < 0.001), less frequently prescribed anticoagulants (p(MG-CG) > 0.05); significantly less often – systemic glucocorticosteroids (p(MG-CG) < 0.001), the group of mucolitic, bronchodilator and antitussive drugs (p(MG-CG) < 0.01), vitamins (p(MG-CG) < 0.001); significantly more often (p(MG-CG) < 0.05) – local antiseptics and the group of the other drugs . There were no significant differences (p(MG-CG) > 0.05) at the second stage of the study in the use of antiviral, immunomodulatory, non-steroidal anti-inflammatory drugs.
Conclusion. Insufficient adherence of medical specialists to recommendations for the treatment of NCI has been established, a number of irrational therapeutic preferences have been identified.
For citation: Bontsevich R.A., Kotlyarova V.K., Bukach O.A., Gubarev A.V., Dubonosova D.G., Rostovceva I.G. Analysis of treatment approaches and the efficiency of application of a decision support program in polyclinic practice during the covid-pandemic period. Meditsinskiy sovet = Medical Council. 2023;(4):77-85. (In Russ.) https://doi.org/10.21518/ms2023-016
Conflict of interest: the authors declare no conflict of interest.
Введение
31 декабря 2019 г. Всемирная организация здравоохранения (ВОЗ) впервые заявила о вспышке пневмонии неизвестной этиологии в китайском городе Ухань. Уже через месяц число заболевших значительно выросло, поэтому ВОЗ объявила вспышку заболевания чрезвычайной ситуацией в области общественного здравоохранения, имеющей международное значение. А уже 11 февраля 2020 г. Международный комитет по таксономии вирусов дал название возбудителю – SARS-CoV-2. Так началась пандемия COVID-19 (новая коронавирусная инфекция – НКИ), унесшая жизни миллионов человек [1, 2].
Распространение НКИ привело к постановке целого ряда важнейших задач перед специалистами здравоохранения и медицинским научным сообществом. Требовалось в короткие сроки изучить клинические и эпидемиологические особенности заболевания, разработать новые средства его профилактики и лечения, уметь быстро диагностировать и оказывать помощь пациентам. На сегодняшний день НКИ распространена повсеместно, а отсутствие единого метода лечения побуждает исследователей и врачей к усовершенствованию лечебных тактик и разработке клинических рекомендаций [3, 4]. Поэтому важно, чтобы первичное звено здравоохранения было знакомо с современными подходами к лечению COVID-19, а также применяло свои знания в практической деятельности. Для достижения этих целей разрабатываются и внедряются в использование программы поддержки принятия врачебных решений (ПППР). Базируясь на современных рекомендациях, ПППР путем унификации действий предназначены улучшить качество оказания медицинской помощи пациентам с COVID-19, ряд из них направлен на устранение необоснованных назначений лекарственных средств (ЛС) [5–9].
Цель исследования – провести анализ назначений ЛС и оценить результаты внедрения ПППР среди врачей-терапевтов и врачей общей практики амбулаторного звена г. Белгорода при лечении НКИ.
Материалы и методы
В рамках данного исследования был проведен анализ схем терапии пациентов с симптомами острого респираторного заболевания, с ПЦР-уточненным (ПЦР – полимеразная цепная реакция) (U07.1 по Международной классификации болезней 10-го пересмотра) и ПЦР-неуточненным (U07.2) диагнозом НКИ, которые обратились за амбулаторной помощью в поликлинические отделения №2, 7 и 8 объединенной поликлиники г. Белгорода в период с августа по ноябрь 2021 г. В ряде случаев пациенты проходили лечение по другим нозологическим единицам, допускающим высокую вероятность инфекции COVID-19, учитывая период пандемии (острая респираторная вирусная инфекция, острый трахеит, острый бронхит, пневмония). Пациенты с подтвержденным диагнозом НКИ были зарегистрированы в COVID-реестре лечебно-профилактического учреждения. Все пациенты имели нетяжелое течение заболевания и не подлежали госпитализации.
В конце сентября 2021 г. в отделениях №2 и 8 была внедрена ПППР (основная группа исследования – ОГ), отделение №7 не использовало ПППР (являлось контрольной группой сравнения – КГ). Данный продукт был разработан Р.А. Бонцевич и др. в 2021 г. на основании временных методических рекомендаций (ВМР) Минздрава России по COVID-19 версий 9–11 [5; 10, c. 39–61] и зарегистрирован в ФГБУ «Федеральный институт промышленной собственности» в феврале 2021 г. [11]. Программа обеспечивала врача базовыми рекомендациями (включая рекомендации по назначению или неназначению антимикробных препаратов (АМП), антикоагулянтов, системных и ингаляционных гормонов), которые с учетом положений ВМР формулировал алгоритм на основе введенных параметров состояния пациента.
В каждой группе все случаи лечения были разделены временным критерием на две подгруппы: до периода внедрения ПППР (подгруппа «До») и после внедрения ПППР (подгруппа «После»).
Были учтены и проанализированы следующие группы ЛС: противовирусные, иммуномодулирующие, антибактериальные средства, антикоагулянты и антиагреганты, муколитики, противокашлевые и бронхолитические ЛС, местные антисептические ЛС, нестероидные противовоспалительные средства (НПВС), глюкокортикоиды, витамины, прочие ЛС.
Внесение информации и анализ данных произведены при помощи программ Microsoft Excel 2019, GraphPad Prism 9 и IBM SPSS Statistics 23. Также в расчетах применялись онлайн-калькуляторы статистических ресурсов. Для сравнения относительных и абсолютных показателей проводился анализ четырехпольных и многопольных таблиц сопряженности с использованием критерия χ2 Пирсона, с помощью которого оценивалась статистическая значимость их различий (фиксировалась при уровне двустороннего р < 0,05). В случаях, когда оценивались малые количества наблюдений (n < 5), рассчитывался точный критерий Фишера либо (при n = 5–9) χ2 Пирсона с поправкой Йейтса.
Результаты и обсуждение
Всего в исследовании было проанализировано 285 амбулаторных эпизодов терапии пациентов с подтвержденным или вероятным COVID-19. Группы были представлены пациентами в возрасте от 18 до 82 лет, из которых 35,1% составили мужчины (100 случаев) и 64,9% – женщины (185 случаев). Характеристика отдельных групп исследования приведена в табл. 1.
На 1-м этапе исследования, с августа по сентябрь 2021 г., до внедрения ПППР общее число проанализированных назначений составило 143 эпизода лечения, из которых ОГ принадлежит 95 случаев, КГ – 48.
Второй этап исследования включал анализ данных на фоне внедрения ПППР в ОГ в октябре – ноябре 2021 г. В КГ и ОГ проанализировано 48 и 94 тактик лечения соответственно.
Таблица 1. Характеристика групп исследования
| Группа | 1-й этап (август – сентябрь 2021 г.) | 2-й этап (октябрь – ноябрь 2021 г.) | ||||
|
n |
Доля мужчин, n, % |
Возраст пациентов, min – max (μ), лет |
n |
Доля мужчин, n, % |
Возраст пациентов, min – max (μ), лет |
|
| Основная |
95 |
32 (33,7%) |
18–80 (41,5) |
94 |
36 (38,3%) |
19–82 (45,0) |
| Контрольная |
48 |
18 (37,5%) |
19–72 (42,4) |
48 |
14 (29,2%) |
19–71 (42,3) |
Основными группами ЛС на 1-м этапе исследования стали:
– противовирусные ЛС (ОГ – 84%; КГ – 93,8%; χ2 = 2,637; p > 0,05);
– иммуномодулирующие ЛС (ОГ – 58,9%; КГ – 85,4%; χ2 = 10,239; p < 0,01);
– витамины (ОГ – 52,6%; КГ – 81,3%; χ2 = 11,11; p < 0,001);
– местные антисептические ЛС (ОГ – 80%; КГ – 68,7%; χ2 = 2,23; p > 0,05);
– НПВС (ОГ – 75,8%; КГ – 68,8%; χ2 = 0,81; p > 0,05);
– прочие ЛС (ОГ – 80%; КГ – 39,6%; χ2 = 23,36; p < 0,001);
– муколитики, противокашлевые и бронхолитические ЛС (ОГ – 37,9%; КГ – 62,5%; χ2 = 7,77; p < 0,01);
– антибактериальные ЛС (ОГ – 24,2%; КГ – 45,8%; χ2 = 6,91; p < 0,01).
Наиболее редко использовались ЛС таких групп, как:
– антикоагулянты и антиагреганты (ОГ – 2,1%; КГ – 4,2%; F = 0,602; p > 0,05);
– глюкокортикоиды (ОГ – 0%; КГ – 10,4%; F = 0,004; p < 0,01).
Результаты 1-го этапа исследования представлены в табл. 2.
Таблица 2. Общая структура назначений лекарственных средств в обеих группах на первом этапе исследования
| Препараты | Случаи назначения группы лекарственных средств, % от количества эпизодов лечения | Количество назначений группы лекарственных средств на один эпизод лечения | ||||
| Основная группа | Контрольная группа | χ2 Пирсона либо точный критерий Фишера (F), p | Основная группа | Контрольная группа | χ2 Пирсона либо точный критерий Фишера (F), p | |
| Противовирусные | 84 | 93,8 | χ2 = 2,64; p > 0,05 | 0,84 | 0,96 | χ2 = 4,49; p > 0,05 |
| Иммуномодулирующие | 58,9 | 85,4 | χ2 = 10,24; p < 0,01 | 0,6 | 0,87 | χ2 = 12,14; p < 0,01 |
| Местные антисептические | 80 | 68,7 | χ2 = 2,23; p > 0,05 | 1,44 | 0,89 | χ2 = 15,47; p < 0,01 |
| Антибактериальные | 24,2 | 45,8 | χ2 = 6,91; p < 0,01 | 0,24 | 0,46 | χ2 = 6,91; p < 0,01 |
| Муколитики, противокашлевые и бронхолитические | 37,9 | 62,5 | χ2 = 7,77; p < 0,01 | 0,54 | 0,96 | χ2 = 9,2; p < 0,01 |
| Нестероидные противовоспалительные средства | 75,8 | 68,8 | χ2 = 0,81; p > 0,05 | 0,77 | 0,69 | χ2 = 1,26; p > 0,05 |
| Глюкокортикоиды | 0 | 10,4 | F = 0,004; p < 0,01 | 0 | 0,1 | F = 0,004; p < 0,01 |
| Антикоагулянты и антиагреганты | 2,1 | 4,2 | F = 0,602; p > 0,05 | 0,02 | 0,04 | F = 0,602; p > 0,05 |
| Витамины | 52,6 | 81,3 | χ2 = 11,11; p < 0,001 | 0,55 | 1,77 | χ2 = 100,9; p < 0,001 |
| Прочие лекарственные средств | 80 | 39,6 | χ2 = 23,36; p < 0,001 | 1,1 | 0,60 | χ2 = 22,31; p < 0,001 |
Согласно ВМР версии 11, которые были актуальны на период исследования, для этиотропного лечения COVID-19 следовало использовать такие препараты, как фавипиравир (коронавир), ремдесивир, умифеновир (арбидол), интерферон α, иммуноглобулин человека против COVID-19 [10, c. 39–61].
Фавипиравир, ремдесивир и умифеновир при анализе данных были отнесены в группу противовирусных ЛС, в которую авторы также отнесли препараты, соответствующие противовирусным по анатомо-терапевтическо-химической классификации и рубрике «фармакологическая группа» инструкции ЛС: имидазолилэтанамид пентандиовой кислоты (Ингавирин®, Витаглутам®), энисамия йодид (Нобазит®), осельтамивира фосфат (Номидес®). В нашем исследовании врачи в большинстве случаев отдавали предпочтение умифеновиру (ОГ – 71,3%; КГ – 65,2%; χ2 = 0,5; р > 0,05), входящему в методические рекомендации, реже – имидазолилэтанамиду пентандиовой кислоты (ОГ – 27,5%; КГ – 10,9%; χ2 = 3,86; р < 0,05), осельтамивира фосфату (ОГ – 0%; КГ – 19,6%; F = 0,00007; р < 0,001), энисамия йодиду (ОГ – 1,3%; КГ – 4,3%; F = 0,55; р > 0,05), которые не входят в рекомендованный перечень препаратов для этиологического лечения НКИ. Также можно отметить, что фавипиравир и ремдесивир на 1-м этапе исследования в назначениях не встречались [10, c. 39–61; 12, с. 38–58].
После внедрения ПППР в ОГ отмечено статистически значимое снижение случаев назначений противовирусных препаратов – с 84 до 71,3% (χ2 = 4,57; p < 0,05). Однако необходимо выделить качественные изменения внутри группы: увеличение эпизодов назначений умифеновира с 71,3 до 80,6% (χ2 = 0,13; p > 0,05) и фавипиравира с 0 до 7,5% (F = 0,03; p < 0,05), а также снижение количества назначений препаратов, не входящих в перечень ВМР по COVID-19, имидазолилэтанамида пентандиовой кислоты с 27,5 до 11,9% (χ2 = 7,59; p < 0,05) и энисамия йодида с 1,3 до 0% (χ2 = 0,99; p > 0,05).
В КГ статистически незначимо изменилось количество эпизодов назначений противовирусных препаратов – с 93,8 до 79,2% (χ2 = 3,203; F = 0,07, p > 0,05), наряду с этим, как и в ОГ, наблюдается тенденция к выбору рекомендованных ВМР препаратов:
– умифеновир – с 65,2 до 81,6% (χ2 = 0,045; p > 0,05);
– фавипиравир – с 0 до 2,6% (χ2 = 2,03; p > 0,05);
– осельтамивира фосфат – с 19,6 до 13,2% (χ2 = 1,34; p > 0,05);
– имидазолилэтанамид пентандиовой кислоты – с 10,9 до 0% (F = 0,028; p < 0,05);
– энисамия йодид – с 4,3 до 2,6% (χ2 = 0,34; p > 0,05).
В обеих группах снижение удельного веса противовирусных ЛС авторы могут связать с присутствием в схемах терапии препаратов интерферона, входящих во ВМР, отнесенных в исследовании к группе иммуномодулирующих ЛС и применяемых в ряде случаев при легком течении без иных этиотропных ЛС [13].
Иммуномодулирующие ЛС назначались специалистами на 1-м этапе исследования в 58,9% случаев в ОГ и в 89,4% в КГ (χ2 = 10,24; р < 0,01). К этой группе были отнесены такие фармакологические препараты, как:
– интерферон α-2b человеческий рекомбинантный (Гриппферон®);
– меглюмина акридонацетат (Циклоферон®);
– тилорон, азоксимера бромид (Полиоксидоний®);
– лизаты бактерий (Бронхо-Мунал®, Исмиген®).
В КГ и ОГ чаще всего был использован интерферон α (ОГ – 94,7%; КГ – 85,7%; F = 0,163; p > 0,05), в свою очередь, среди перечисленных это единственный препарат, который рекомендован для лечения НКИ. Статистически значимых изменений в частоте применения препаратов данной группы после внедрения ПППР не было выявлено (р(ОГ-КГ) > 0,05): изменение в ОГ с 58,9 до 67% (χ2 = 1,32; p > 0,05), в КГ – c 85,4 до 77,1% (χ2 = 1,09; p > 0,05).
Антибактериальные ЛС (АМП) неактивны в отношении SARS-CoV-2 – вирусной инфекции, в связи с этим их использование может быть расценено как нерациональное, за исключением наличия убедительных признаков присоединения бактериальной инфекции: повышение прокальцитонина более 0,5 нг/мл, появление гнойной мокроты, лейкоцитоз более 12 × 109/л (при отсутствии предшествующего применения глюкокортикоидов), повышение числа палочкоядерных нейтрофилов более 10% [10, c. 39–61]. Несоблюдение принципов рационального применения АМП способствует росту устойчивости микроорганизмов к ЛС, что является глобальной проблемой для мирового сообщества [14].
По результатам 1-го этапа исследования АМП назначались в 24,2% (ОГ) и 45,8% (КГ) случаев (χ2 = 6,91; p < 0,01). Авторы связывают данные различия с вероятным влиянием проводимых ранее (в 2020 г.) образовательных программ по рациональной антимикробной терапии в отделениях поликлиники №2 и 8 (Т.М. Шагиева, Р.А. Бонцевич). Наибольшее предпочтение отдавалось следующим препаратам:
– амоксициллин + клавулановая кислота (Амоксиклав®, Аугментин®) (ОГ – 56,5%; КГ – 77,3%; χ2 = 1,35; p > 0,05);
– азитромицин (Суммамед®) (ОГ – 30,4%; КГ – 13,6%; F = 0,284; p > 0,05).
Также были использованы такие препараты, как:
– левофлоксацин (ОГ – 4,4%; КГ – 0%; F = 1; p > 0,05);
– цефиксим (ОГ – 4,4%, КГ– 0%; F = 1; p > 0,05);
– цефтриаксон (ОГ – 4,4%; КГ – 9,1%; F = 0,608; p > 0,05).
Весьма показательные результаты получены при анализе частоты назначений АМП после внедрения ПППР. В ОГ даже при исходно достаточно низком уровне статистически значимо снизились случаи назначения АМП – с 24,2 до 6,4% (χ2 = 11,56; p < 0,001). Различия с КГ стали еще более значимыми (χ2 = 15,63; p < 0,001). Внутри группы произошло перераспределение ЛС: по сравнению с 1-м этапом увеличилось количество назначений азитромицина – с 30,4 до 50% (F = 0,38; p > 0,05) и левофлоксацина – с 4,4 до 16,7% (F = 0,37; p > 0,05), количество других препаратов уменьшилось: амоксициллин + клавулановая кислота – с 56,5 до 33,3% (F = 0,39; p > 0,05), цефалоспорины III поколения (цефиксим, цефтриаксон) больше не назначались (F = 1; p > 0,05). В КГ статистически значимых изменений в назначении АМП не было выявлено, хотя и было отмечено снижение частоты назначений АМП с 45,8 до 33,3% (χ2 = 1,57; p > 0,05).
Один из механизмов патогенетического воздействия на организм вируса НКИ заключается в неконтролируемой активации эндогенных иммуномодуляторов, приводящих к развитию системной воспалительной реакции, или цитокинового шторма, что, в свою очередь, определяет тяжелое течение заболевания [15]. Гипериммунная реакция является точкой приложения иммуносупрессивных препаратов – генноинженерных биологических препаратов и (или) глюкокортикоидов. В нашем исследовании назначений на уровне амбулаторно-поликлинического звена использовались только глюкокортикоиды. До внедрения ПППР в ОГ глюкокортикоиды не назначались, в КГ частота применения составила 10,4% (F = 0,004; р < 0,01), из которых чаще применялся дексаметазон (80%) и реже будесонид (Пульмикорт®) – 20%. Действующие на данный период ВМР гласят, что для патогенетического воздействия при легкой форме инфекции не рекомендуется использовать глюкокортикоиды для внутривенного и перорального применения, при этом возможно применение ингаляционных форм глюкокортикоидов в качестве дополнительной терапии [10, c. 39–61; 12, с. 38–58; 16, с. 6–63; 17].
После внедрения ПППР значительного увеличения случаев применения глюкокортикоидов не обнаружено при значимых различиях между ОГ и КГ (3,2% и 23%, р(ОГ-КГ) < 0,001): в ОГ установлено изменение частоты назначений с 0 до 3,2% (F = 0,12; p > 0,05), среди которых применялись только ингаляционные формы глюкокортикоидов (будесонид – 100%); в КГ – с 10,4 до 23% (χ2 = 1,87; p > 0,05), а также произошли качественные изменения внутри группы: дексаметазон стал применяться реже – с 80 до 46,2% (F = 0,31; p > 0,05), а будесонид – чаще: с 20 до 53,8% (F = 0,31; p > 0,05). Таким образом, в КГ значимо чаще были использованы системные глюкокортикоиды (в 6 раз чаще в сравнении с их отсутствием в ОГ, F = 0,001; р < 0,01), что необоснованно в амбулаторной практике при нетяжелой форме НКИ.
Применение прямых пероральных антикоагулянтов (ривароксабан, апиксабан или дабигатрана этексилат), низкомолекулярного гепарина рекомендовано для пациентов со среднетяжелой формой НКИ и высоким риском тромбоза глубоких вен нижних конечностей и тромбоэмболии легочной артерии [10, c. 39–61]. Специалисты ОГ прописывали антикоагулянты на 1-м этапе в 2,1% случаев, на 2-м этапе увеличилось количество назначений до 9,6% (статистическая значимость в пограничном диапазоне в зависимости от применяемой статистики: F = 0,023, p < 0,05; χ2 = 3,54, p > 0,05). В КГ произошло увеличение в случаях назначений с 4,2% на 1-м этапе до 18,8% на 2-м (F = 0,05, p > 0,05; χ2 = 3,69, p > 0,05). Между ОГ и КГ выявленные различия не были значимыми (F = 0,602, p > 0,05 – 1-й этап; χ2 = 1,66, p > 0,05 – 2-й).
Остальные группы ЛС для обсуждения можно отнести к симптоматическому лечению COVID-19. К ним относятся НПВС, муколитические, противокашлевые и бронхолитические ЛС, местные антисептические и прочие ЛС.
НПВС применялись специалистами амбулаторного звена до внедрения ПППР достаточно часто: в 75,8% случаев в ОГ и в 68,8% в КГ (χ2 = 0,81, p > 0,05). Из жаропонижающих ЛС преимущественно назначался парацетамол (ОГ – 53,4%; КГ – 78,8%; χ2 = 6,16, p < 0,05). Назначение других НПВС при НКИ распределилось следующим образом:
– Ибуклин® (ОГ – 37%; КГ – 13,8%; χ2 = 11,79, p < 0,001);
– Анальгин® (ОГ – 6,8%; КГ – 18,2%; F = 0,09, p > 0,05);
– ибупрофен (ОГ – 1,4%; КГ – 0%; F = 1, p > 0,05);
– нимесулид (ОГ – 1,4%; КГ – 0%; F = 1, p > 0,05).
После анализа данных 2-го этапа достоверных изменений среди назначений ЛС данной группы выявлено не было (ОГ – 66%, χ2 = 2,21, p > 0,05; КГ – 60,4%, χ2 = 0,73, p > 0,05; р(ОГ-КГ) > 0,05).
Для комплексной терапии симптомов бронхита при НКИ респонденты прописывали муколитические, противокашлевые и бронхолитические ЛС в ОГ и КГ в 37,9 и 62,5% случаев соответственно (χ2 = 7,768, p < 0,05). В ОГ по данным 1-го этапа наиболее часто назначался амброксол (31,5%), в КГ – грудной сбор №4 (28,3%), при этом грудной сбор в 100% случаях назначался совместно с любым другим препаратом исследуемой группы.
На 2-м этапе исследования ЛС данной группы врачи назначали чаще – в 44,7% случаев в ОГ и в 70,8% в КГ (χ2 = 8,736, p < 0,05). Статистически значимых структурных изменений в назначениях врачей-специалистов не было выявлено, общая частота назначений данных ЛС в ОГ возросла с 37,9 до 44,7% (χ2 = 0,898; p > 0,05), в КГ – с 62,5 до 70,8% (χ2 = 0,75; p > 0,05). Структура назначений препаратов в обеих группах представлена на рис. 1.
Рисунок 1. Доля назначения препаратов из категории муколитических, противокашлевых и бронхолитических лекарственных средств в исследуемых группах, %
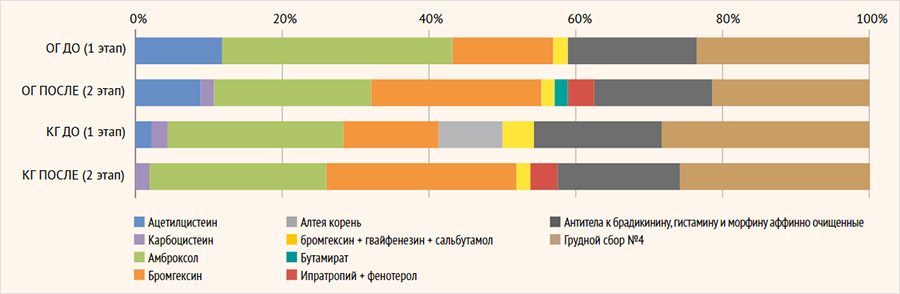
ОГ – основная группа; КГ – контрольная группа; ДО – до периода внедрения программы поддержки принятия врачебных решений; ПОСЛЕ – после периода внедрения программы поддержки принятия врачебных решений.
Местные антисептические препараты встречались в назначениях специалистов на 1-м этапе исследования достаточно часто: ОГ – 80%, КГ – 68,8% (χ2 = 2,23, p > 0,05). При развитии таких симптомов, как першение и боль в горле, согласно ВМР, вполне оправданно применение солевых растворов или растворов с антисептическим действием в виде полосканий, спреев, ингаляций и таблеток, леденцов для рассасывания. Местное антисептическое воздействие на ротоглотку способствует снижению концентрации вируса и профилактике присоединения бактериальной суперинфекции при острой респираторной вирусной инфекции [10, c. 39–61; 12, с. 38–58; 16, с. 6–63; 18]. Внутри группы местных антисептических ЛС препараты были разделены по принципу химического строения: в ОГ врачи чаще назначали производные нитрофуранов (Фурацилин®, Фуразидин®) – 37,3% и гипертонический раствор морской воды (Аквалор®) – 24,8%; в КГ отдавали предпочтение ЛС, содержащим бензидамин (Тантум Верде®, Ангидак®, Оралсепт®) – 41,9% и гексэтидин (Гексорал®) – 30,2%. После внедрения ПППР в ОГ статистически достоверных количественных и качественных изменений не было выявлено, частота применения ЛС не изменилась (80 и 80,4%, χ2 = 0,02; p > 0,05), как и в КГ (68,8 и 62,5%, χ2 = 0,42; p > 0,05), однако выявлена значимая разница между ОГ и КГ (χ2 = 5,65, p < 0,05).
В перечень прочих ЛС вошли следующие ЛС:
– α-адреномиметики;
– пробиотики;
– антигистаминные препараты;
– диоксометилтетрагидропиримидин (Метилурацил®);
– препараты растительного происхождения (ромашка, календула, Ротокан®, отвар коры дуба).
Авторами выявлено, что статистически значимых изменений в динамике в группе прочих ЛС не было: на 1-м этапе исследования в ОГ данные препараты назначали в 80% случаев, на 2-м этапе – в 72,3% (χ2 = 1,53; p > 0,05); в КГ в 39,6 и 52% случаев на 1-м и 2-м этапе соответственно (χ2 = 1,51; p > 0,05). Между ОГ и КГ установлены значимые различия (1-й этап – χ2 = 23,36, p < 0,001; χ2 = 5,77, p < 0,05), анализ причин различий в данной неоднородной и неосновной в лечении НКИ группы ЛС не входил в задачи исследования.
Последняя группа для обсуждения, но довольно часто встречающаяся среди назначений – витамины (ОГ – 52,6%; КГ – 81,3% на 1-м этапе, χ2 = 11,11, p < 0,001). Лидирующую позицию в ОГ занимает аскорбиновая кислота (витамин С) – 80,8%; в КГ первенство делят между собой витамины С (38,8%) и D (35,3%). Кроме того, врачи применяли витамин Е (ОГ – 1,9%; КГ – 0%), Аскорутин® (ОГ – 0%; КГ – 15,3%), Аевит® (ОГ – 0%; КГ – 8,2%), поливитамины (ОГ – 5,8%; КГ – 2,4%). В связи с отсутствием доказательной базы в отношении положительного влияния на течение острой респираторной вирусной инфекции, вызванной SARS-CoV-2, рутинное назначение витаминов не несет практической пользы и требует дальнейшего исследования [19]. Разница прироста в назначениях врачами-специалистами между двумя этапами исследования статистически не значима: ОГ (52,6 и 62,6%, χ2 = 1,233; p > 0,05), КГ (81,3 и 87,5%, F = 0,575; p > 0,05), в то же время между ОГ и КГ разница оказалась значимой на обоих этапах (1-й – χ2 = 11,11, p < 0,001; 2-й – χ2 = 10,86, p < 0,001).
На рис. 2 приведены данные по динамике назначений основных групп ЛС, применяемых врачами для терапии НКИ.
Рисунок 2. Назначения лекарственных средств на первом и втором этапе исследования
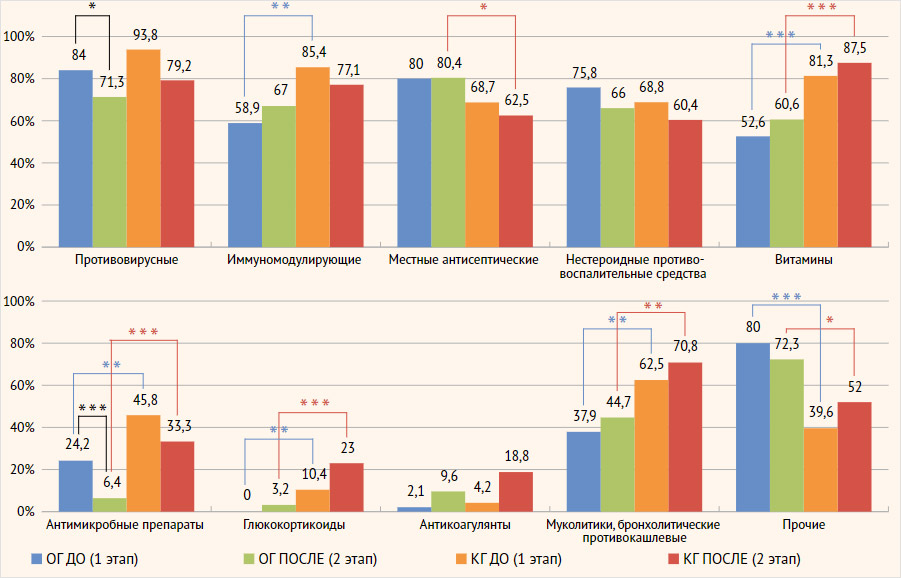
ОГ – основная группа; КГ – контрольная группа; ДО – до периода внедрения программы поддержки принятия врачебных решений; ПОСЛЕ – после периода внедрения программы поддержки принятия врачебных решений.
* – p < 0,05. ** – p < 0,01. *** – p < 0,001.
Таким образом, в период исследования был выявлен ряд статистически значимых различий между ОГ и КГ в назначениях ЛС. Наиболее важными авторы считают достоверное снижение уровня назначаемых АМП в ОГ на фоне внедрения ПППР (даже при наличии исходно более низкого уровня применения АМП в ОГ) при отсутствии значимой динамики в КГ.
Можно предположить, что прочие различия были связаны как с внедрением ПППР в ОГ, так и другими факторами, такими как работа руководителей подразделений, предыдущие образовательные мероприятия, различные индивидуальные знания и предпочтения врачей. Такие различия встречаются в группах местных антисептических, антибактериальных ЛС, муколитиков, противокашлевых и бронхолитических ЛС, глюкокортикоидов, витаминов и прочих ЛС. Сводная структурная характеристика назначений ЛС на 2-м этапе представлена в табл. 3.
Таблица 3. Общая структура назначений лекарственных средств в обеих группах на втором этапе исследования
| Препараты | Случаи назначения группы лекарственных средств, % от количества эпизодов лечения | Количество назначений группы лекарственных средств на один эпизод лечения | ||||
| Основная группа | Контрольная группа | χ2 Пирсона либо точный критерий Фишера (F), p | Основная группа | Контрольная группа | χ2 Пирсона либо точный критерий Фишера (F), p | |
| Противовирусные | 71,3 | 79,2 | χ2 = 1,027; p > 0,05 | 0,71 | 0,79 | χ2 = 1,027; p > 0,05 |
| Иммуномодулирующие | 67 | 77,1 | χ2 = 1,54; p > 0,05 | 0,73 | 0,77 | χ2 = 5,45 p > 0,05 |
| Местные антисептические | 80,4 | 62,5 | χ2 = 5,65; p < 0,05 | 1,31 | 0,86 | χ2 = 9,08; p > 0,05 |
| Антибактериальные | 6,4 | 33,3 | χ2 = 15,63; p < 0,001 | 0,06 | 0,33 | χ2 = 15,63; p < 0,001 |
| Муколитики, противокашлевые и бронхолитические | 44,7 | 70,8 | χ2 = 8,74; p < 0,01 | 0,6 | 1,13 | χ2 = 17,51; p < 0,001 |
| Нестероидные противовоспалительные средства | 66 | 60,4 | χ2 = 0,42; p > 0,05 | 0,66 | 0,6 | χ2 = 0,42; p > 0,05 |
| Глюкокортикоиды | 3,2 | 23 | F = 0,0004; p < 0,001 | 0,03 | 0,27 | χ2 = 14,39; p < 0,001 |
| Антикоагулянты и антиагреганты | 9,6 | 18,8 | χ2 = 1,66; p > 0,05 | 0,1 | 0,19 | χ2 = 1,66; p > 0,05 |
| Витамины | 60,6 | 87,5 | χ2 = 10,86; p < 0,001 | 0,71 | 1,75 | χ2 = 67,92; p < 0,001 |
| Прочие лекарственных средств | 72,3 | 52 | χ2 = 5,77; p < 0,05 | 1 | 0,69 | χ2 = 8,01; p > 0,05 |
Заключение
В ходе исследования определена структура назначений и выявлен ряд нерациональных терапевтических предпочтений среди врачей амбулаторного звена, касающихся лечения НКИ. На фоне внедрения ПППР специалисты статистически значимо уменьшили необоснованное назначение антибактериальных препаратов. Также в ОГ выявлена более низкая частота назначения антикоагулянтов и системных глюкокортикоидов, что обычно обосновано в случае с нетяжелой ковид-инфекцией и соответствует рекомендациям по лечению данного заболевания.
Также авторы выявили тенденцию к избыточному назначению ряда препаратов, не имеющих достаточного теоретического обоснования к применению при лечении SARS-CoV-2 и не включенных в рекомендации, что может увеличить риск нежелательных лекарственных реакций и снижает комплаентность пациентов. Мы предполагаем, что дальнейшие врачебные образовательные мероприятия, совершенствование и рациональное использование ПППР помогут улучшить качество ведения пациентов с НКИ.
Список литературы / References
- Авдеев С.Н., Адамян Л.В., Алексеева Е.И., Багненко С.Ф., Баранов А.А., Баранова Н.Н. и др. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19): временные методические рекомендации. Версия 15 (22.02.2022). М.; 2022. 245 с. Режим доступа: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/059/392/original/ВМР_COVID-19_V15.pdf.
- Asselah T., Durantel D., Pasmant E., Lau G., Schinazi R.F. COVID-19: Discovery, diagnostics and drug development. J Hepatol. 2021;74(1):168-184. https://doi.org/10.1016/j.jhep.2020.09.031.
- Pascarella G., Strumia A., Piliego C., Bruno F., Del Buono R., Costa F. et al. COVID-19 diagnosis and management: a comprehensive review. J Intern Med. 2020;288(2):192-206. https://doi.org/10.1111/joim.13091.
- Bontsevich R., Vovk Y., Solovyova L. Practical experience in optimizing COVID-19 therapy in an outpatient setting. Eur Respir J. 2021;58(Suppl. 65):PA3677. https://doi.org/10.1183/13993003.congress-2021.PA3677.
- Бонцевич Р.А. Разработка и внедрение программы поддержки врачебных решений в амбулаторной практике работы с ковид-19-инфекцией. В: Батищева Г.А. (ред.). Актуальные вопросы лекарственного обеспечения и контроль качества препаратов: сборник трудов научно-практической конференции, Воронеж, 27 мая 2021 г. Воронеж: Воронежский государственный медицинский университет имени Н.Н. Бурденко; 2021. С. 85-87. Режим доступа: https://www.elibrary.ru/item.asp?id=47353450&pff=1.
- Salah H.A., Ahmed A.S. Coronavirus Disease Diagnosis, Care and Prevention (COVID-19) Based on Decision Support System. Baghdad Sci J. 2021;18(3):0593. https://doi.org/10.21123/bsj.2021.18.3.0593.
- Catho G., Centemero N.S., Catho H., Ranzani A., Balmelli C., Landelle C. et al. Factors determining the adherence to antimicrobial guidelines and the adoption of computerised decision support systems by physicians: A qualitative study in three European hospitals. Int J Med Inform.2020;141:104233. https://doi.org/10.1016/j.ijmedinf.2020.104233.
- Ray J.M., Wong A.H., Yang T.J., Buck S., Joseph M., Bonz J.W. et al. Virtual Telesimulation for Medical Students During the COVID-19 Pandemic. Acad Med. 2021;96(10):1431-1435. https://doi.org/10.1097/ACM.0000000000004129.
- Moulaei K., Bahaadinbeigy K. Diagnosing, Managing, and Controlling COVID-19 using Clinical Decision Support Systems: A Study to Introduce CDSS Applications. J Biomed Phys Eng. 2022;12(2):213-224. https://doi.org/10.31661/jbpe.v0i0.2105-1336.
- Авдеев С.Н., Адамян Л.В., Алексеева Е.И., Багненко С.Ф., Баранов А.А., Баранова Н.Н. и др. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19): временные методические рекомендации. Версия 11 (07.05.2021). М.; 2021. 225 с. Режим доступа: https://стоп-коронавирус.рф/ai/doc/872/attach/Bmr_COVID-19_compressed.pdf.
- Бонцевич Р.А., Коренев И.В., Батищева Г.А., Покровский М.В. Программа поддержки принятия врачебных решений (вариант исполнения - «Амбулаторная помощь при COVID19»). Свидетельство о государственной регистрации программы для ЭВМ №2021612652 РФ, 20.02.2021. Режим доступа: https://www.fips.ru/ofpstorage/Doc/PrEVM/RUNWPR/000/002/021/612/652/2021612652-00001/document.pdf.
- Авдеев С.Н., Адамян Л.В., Алексеева Е.И., Багненко С.Ф., Баранов А.А., Баранова Н.Н. и др. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19): временные методические рекомендации. Версия 12 (21.09.2021). М.; 2021. 232 c. Режим доступа: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/058/075/original/ВМР_COVID-19_V12.pdf.
- Бонцевич Р.А., Винюков В.А., Вовк Я.Р., Субина Т.Л., Дубоносова Д.Г. Предпочтения врачей-терапевтов в выборе противовирусных и иммуномодулирующих средств в период пандемии COVID-19. В: Максимов М.Л., Шикалева А.А., Исмаилова М.А. (ред.). Сборник трудов конференции IV Всероссийской научно-практической конференции с международным участием «Безопасность фармакотерапии: NOLI NOCERE!», Казань, 20 мая 2021 г. Казань: МеДДок; 2021. С. 27. Режим доступа: https://www.elibrary.ru/item.asp?id=46548716.
- Bontsevich R., Vinyukov V., Subina T., Vovk Y., Dubonosova D. The frequency of prescribing antimicrobial drugs in the initial therapy of COVID-19 at the outpatient stage. Eur Respir J. 2021;58(Suppl. 65):PA3675. https://doi.org/10.1183/13993003.congress-2021.PA3675.
- Щелканов М.Ю., Колобухина Л.В., Бургасова О.А., Кружкова И.С., Малеев В.В. COVID-19: этиология, клиника, лечение. Инфекция и иммунитет. 2020;10(3):421-445. https://doi.org/10.15789/2220-7619-CEC-1473.
- Авдеев С.Н., Адамян Л.В., Алексеева Е.И., Багненко С.Ф., Баранов А.А., Баранова Н.Н. и др. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19): временные методические рекомендации. Версия 13 (14.10.2021). М.; 2021. 237 c. Режим доступа: https://static-0.minzdrav.gov.ru/system/attachments/attaches/000/058/211/original/BMP-13.pdf.
- Рута А.В., Лучинина Е.В., Шелехова Т.В., Зайцева М.Р., Лучинин Е.А., Бонцевич Р.А. Влияние преднизолона на биомаркеры воспаления при интерстициальной пневмонии, сопряженной с коронавирусной инфекцией. Актуальные проблемы медицины. 2022;45(2):129-140. https://doi.org/10.52575/2687-0940-2022-45-2-129-140.
- Саливончик Е.И., Саливончик Д.П. Современные аспекты лечения острых респираторных инфекций верхних дыхательных путей в период COVID-19. Оториноларингология. Восточная Европа. 2021;11(1):93-106. https://doi.org/10.34883/PI.2021.11.1.046.
- Milani G.P., Macchi M., Guz-Mark A. Vitamin C in the Treatment of COVID-19. Nutrients. 2021;13(4):1172. https://doi.org/10.3390/nu13041172.






