
Журнал "Медицинский совет" №18/2021
DOI: 10.21518/2079-701X-2021-18-192-201
М.Ю. Коркмазов1, ORCID: 0000-0002-8642-0166
М.С. Ангелович1, ORCID: 0000-0002-2848-4313
М.А. Ленгина1, ORCID: 0000-0002-8103-192X
А.П. Ястремский2, ORCID: 0000-0002-7760-4860
1 Южно-Уральский государственный медицинский университет; 454092, Россия, Челябинск, ул. Воровского, д. 64
2 Тюменский государственный медицинский университет; 625023, Россия, Тюмень, ул. Одесская, д. 54
Введение. Необходимость закрытия ликворных свищей в ранние сроки связано с высоким риском возникновения внутричерепных осложнений. Определенные сложности закрытия костных дефектов обусловлены вариабельностью точной локализации свищевого канала, выбором операционного доступа, надежностью пластического материала. В литературе описаны различные методы устранения базальных ликворей, однако преимущество ни одного из них не доказано, что обуславливает актуальность поиска новых методик.
Цель. На основе изучения отдаленных результатов повысить эффективность пластического закрытия ликворных свищей с использованием высокоинтенсивного лазерного излучения.
Материалы иметоды. Проведен анализ эффективности 15-летнего опыта пластического закрытия ликворных свищей у 126 прооперированных пациентов с базальной ликвореей. Длительность заболевания составляла от 2 мес. до 1,5 лет. Основную группу составили 94 пациента, которым пластическое закрытие ликворных свищей осуществлялось с использованием высокоинтенсивного лазерного излучения длиной волны 0,97 мкм и мощностью 2,5–3,5 Вт. Контрольную группу составили 32 пациента, которым когерентное лазерное излучение не применялось. В дополнение к общепринятым методам послеоперационного ведения всем пациентам для ускорения репаративных процессов использовали низкочастотное ультразвуковое кавитационное орошение оперированных полостей.
Результаты и обсуждение. Средний срок наблюдения после хирургического закрытия ликвореи составил более 13 лет. При сопоставлении результатов лечения главным критерием оценки эффективности операции являлась частота рецидивов. В 15 (12,3%) случаях отмечен рецидив, из них у 5 (3,71%) пациентов основной группы и у 10 (8,32%) пациентов группы контроля, которые были закрыты повторным хирургическим вмешательством.
Выводы. К клиническим особенностям ликворных фистул можно отнести вариабельность локализации свищевых каналов, определенные трудности их обнаружения, большое разнообразие способов пластического закрытия, высокий процент рецидивов. Проведенное проспективное неконтролируемое исследование показало, что данный способ пластики ликворных фистул позволяет повысить эффективность оперативного лечения.
Для цитирования: Коркмазов М.Ю., Ангелович М.С., Ленгина М.А., Ястремский А.П. Пятнадцатилетний опыт пластики ликворных свищей с применением высокоинтенсивного лазерного излучения. Медицинский совет. 2021;(18):192–201. https://doi.org/10.21518/2079-701X-2021-18-192-201.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Fifteen years of experience in plastic liquor fistulas using high-intensity laser radiation
Musos Yu. Korkmazov1, ORCID: 0000-0002-8642-0166
Mihail S. Angelovich1, ORCID: 0000-0002-2848-4313
Maria A. Lengina1, ORCID: 0000-0002-8103-192X
Andrey P. Yastremsky2, ORCID: 0000-0002-7760-4860
1 South Ural State Medical University; 64, Vorovskogo St., Chelyabinsk, 454092, Russia
2 Tyumen State Medical University; 54, Odesskaya St., Tyumen, 625023, Russia
Introduction. The need to close liquor fistulas as early as possible is associated with a high risk of intracranial complications. Certain difficulties in closing bone defects are due to the variability of the exact localization of the fistulous canal, the choice of the surgical approach, and the reliability of the plastic material. The literature describes various methods for eliminating basal liquorrhea, however, the advantage of none of them has not been proven, which determines the relevance of the search for new methods.
Objective. Based on the analysis of long-term results, to study the efficiency of plastic closure of cerebrospinal fluid fistulas using high-intensity laser radiation.
Materials and methods. An analysis of 15 years of experience in studying the effectiveness of plastic closure of cerebrospinal fluid fistulas in 126 operated patients with basal liquorrhea was carried out. The duration of the disease ranged from 2 months to 1.5 years. The main group consisted of 94 patients who underwent plastic closure of CSF fistulas using high-intensity laser radiation with a wavelength of 0.97 μm and a power of 2.5–3.5 W. The control group consisted of 32 patients who did not receive coherent laser radiation. In addition to the generally accepted methods of postoperative management, low-frequency ultrasonic cavitation irrigation of the operated cavities was used to accelerate the reparative processes in all patients.
Results and discussion. The average follow-up period after surgery was over 13 years. When comparing the results of treatment, the main criterion for evaluating the effectiveness of the operation was the frequency of relapses. In 15 (12.3%) cases, a relapse was noted, of which 5 (3.71%) were patients in the main group and in 10 (8.32%) patients in the control group, who were closed by repeated surgery.
Conclusion. The clinical features of the basal liquorrhea include the variability in the localization of the fistulous canals, certain difficulties in their detection, a wide variety of plastic closure methods, and a high percentage of relapses. A prospective uncontrolled study has shown that this method of CSF fistula plasty using improves the efficiency of surgical treatment.
For citation: Korkmazov M.Yu., Angelovich M.S., Lengina М.А., Yastremsky А.Р. Fifteen years of experience in plastic liquor fistulas using high-intensity laser radiation. Meditsinskiy sovet = Medical Council. 2021;(18):192–201. (In Russ.) https://doi.org/10.21518/2079-701X-2021-18-192-201.
Conflict of interest: the authors declare no conflict of interest.
Введение
Под определением назальная ликворея (НЛ) понимается истечение через дефекты ликворных пространств полости черепа цереброспинальной жидкости. Первые упоминания о НЛ относятся к середине II в. н. э.: С. Galenus описывает ликворею как преходящее нормальное физиологическое состояние, когда ликвор истекает через решетчатую кость при различных заболеваниях человека [1]. Видимо, такое мнение было связано с наличием у пациентов вазомоторных или аллергических ринитов, гипертрофических процессов носовых раковин. Позднее, в 1676 г., Th. Willis предложил первые классификации НЛ, которые немного расширил G. Bidloo в 1710 г. в своих трудах «для изучающих хирургию в анатомическом театре». В 1899 г. St.С. Thompson опубликовал более четкие представления о различных видах НЛ, связывая их в большей части с черепно-мозговой травмой, и впервые предложил дифференциальную диагностику обычной ринореи и НЛ [2].
В настоящее время лечение больных с НЛ различной этиологии является одним из актуальных вопросов оториноларингологии и смежных специальностей, таких как неотложная хирургия, нейрохирургия. Связано это, прежде всего, с ростом количества больных на стационарном лечении, поступающих не только с тяжелыми черепно-мозговыми и сочетанными травмами, но и со спонтанной и ятрогенной НЛ [3, 4].
Как правило, чаще этиологическими составляющими НЛ, в т.ч. спонтанных форм, могут являться повышение внутричерепного давления, врожденные дефекты основания черепа, гиперпневматизированные околоносовые пазухи, синдром пустого турецкого седла, ожирение, остеопороз и т.д. [4, 5].
По данным отдельных авторов, эпидемиологически среди всех черепно-мозговых травм т. н. базальные ликвореи (БЛ) сопровождаются в 80–90% случаях при краниофациальных повреждениях, переломах основания черепа с переходом на пирамиду височной кости и повреждением твердой мозговой оболочки, переломах церебральных стенок околоносовых пазух [3, 5, 6]. Нередким проявлением БЛ могут быть как повреждения в области дна передней черепной ямки, черепно-мозговые и спинномозговые грыжи различной этиологии, опухоли, растущие инвазивно у основания черепа, так и ликвореи вследствие оториноларингологических и нейрохирургических оперативных вмешательств [7, 8].
Патогенетические механизмы возникновения ликворей сложны и многообразны, основаны на характере сопутствующих патологических состояний или полученных травм. Так, например, околоносовые пазухи вовлекаются при передних краниобазальных повреждениях, в то время как ушные ликвореи – при травмах пирамиды и ячеек сосцевидного отростка височной кости [9, с. 158– 198]. Поскольку основную причину ликвореи определяют дефект костной стенки и повреждение мозговых оболочек, в настоящее время выделяют три пути реализации, к которым относятся формирование с отсутствием регенерации дефекта, обширные разрывы и ущемление оболочек костными отломками. Пролабирование мозговых оболочек через сформированные костные диастазы препятствует заращению, создает предпосылки внутричерепных инфекционных осложнений, образуя мозговые грыжи.
По локализации источников ринореи через дуральные фистулы доминирующее месторасположение занимают ячейки решетчатой кости, затем переломы лобных пазух и на третьем месте находятся травмы основной пазухи, что прежде всего связано с тесным прилежанием паутинной оболочки и малой прочностью этмоидальных пластинок. Кроме того, ликвореи могут возникнуть при отсутствии костных дефектов, например при отрыве волокон olfactory nerve через отверстия ситовидной пластинки решетчатой кости при травмах.
Из всех предложенных классификаций, наиболее полно отражающих этиопатогенетические аспекты ликворей, является классификация, предложенная в клинических рекомендациях В.А. Охлопкова в 2015 г., в которой по этиологии выделяют черепно-мозговые травмы и ятрогенные ликвореи, а по времени возникновения – немедленные и отсроченные; последние, в свою очередь, делятся на ранние (ликворея проявляется до одного месяца) и более поздние, возникающие через один месяц и более. По частоте локализации ликворных свищей на первом месте находится ситовидная пластинка и сама решетчатая кость, затем по мере убывания – фронтальная и сфеноидальная пазухи, крыша орбиты. Кроме того, имеется разделение по латерализации свищей – одно- или двусторонние, по расположению по средней линии, справа или слева, а по количеству фистул – одна или более, по истечению ликвора – назальные, носоглоточные, глазничные, парадоксальные, ушные, смешанные и т. д. По объему истечения в указанной классификации выделяются три показателя: до 1 мл в сутки – скудный, до 30 мл в сутки – умеренный и 30 мл и более – профузный. По типу ликвореи выделяют явную и скрытую, по времени истечения – периодическую и постоянную, по клиническому течению – осложненную и неосложненную. Таким образом, основная задача классификации – помочь врачу правильно верифицировать диагноз «НЛ» на этапах маршрутизации пациента, отработать наиболее оптимальную тактику персонализированного консервативного или хирургического лечения больного.
Для успешной ликвидации НЛ необходимо проводить достоверную локализацию ликворного свища. В этом контексте применяется комплексный подход диагностики НЛ, который начинается с подробного сбора жалоб пациента, проведения Halo-теста, тщательной эндовидеориноскопии. В дальнейшем для точного определения фистулы по возможности проводится тест флюоресцеином, биохимический анализ назального ликворного отделяемого (определение бета-2-трансферрина электрофорезом в полиакриламидном геле и иммуноблоттингом), КТ, МРТ, КТ- и МР-цистернография, иммунологические тесты [10–15]. В современных литературных источниках описываются случаи местонахождения ликворных фистул в лобной пазухе – 6,7%, ситовидной пластинке решетчатой кости – 40%, этмоидальных ячейках – 30%, сфеноидальной пазухе – 10% и при множественных дефектах в различных местах основания черепа – 13,3% [3, 8, 14]. Использование в клиниках, оснащенных вышеуказанным современным диагностическим оборудованием, делает возможным верификацию зон костных дефектов и фистулы, точную локализацию свищевого хода за счет регистрации контрастного вещества в зоне ЛС, характера затекания ликвора в полость носа и околоносовых пазух.
Несомненно, основной задачей всех научных исследований является совершенствование диагностики локализаций НЛ, оказание лечебного пособия, повышение качества жизни пациентов. Так, в 1952 г. в поисках новых, менее инвазивных методик О. Гирш впервые успешно произвел закрытие ликворного свища с применением эндоскопа. В 1981 г. M.E. Wigand впервые применил эндоназальный доступ с использованием ригидных эндоскопов при пластике интраоперационных повреждений твердой мозговой оболочки [16]. Более полную информацию хирургического лечения НЛ, основанную на обширной базе литературных данных и собственного опыта, представил в 2015 г. А.И. Крюков [17, 18]. В настоящее время наличие в хирургических стационарах современного оптического оборудования, позволяющего проводить более качественный обзор операционного поля, и необходимого хирургического инструментария делает возможным для хирургов осуществлять манипуляции в труднодоступных анатомических местах. Возможности малоинвазивных эндоскопических хирургических методик широко применяются при закрытии ликворных фистул ситовидной пластинки и всех околоносовых пазухах [1, 6, 17, 19] с учетом механизма возникновения ликворных фистул и их локализации. К настоящему времени разработаны и внедрены в практическую медицину различные методики и варианты операционных доступов для устранения НЛ. Так, например, в ГБУЗ НИКИО им. Л.И. Свержевского разработаны методы: а) послойная пластика области свищевого дефекта после предварительной обработки и укладки тахокомба, затем герметика (Duraseal Bioglue, Tissucol), на которую укладывается опять тахокомб и гемостатическая губка и/или салфетка суржецел; б) сформированная культя из средней носовой раковины (свободный костнослизистый лоскут нижней носовой раковины) укладывается на слизисто-надкостничный лоскут перегородки носа и прикрывается герметиком (Duraseal Bioglue, Tissucol), на котрый укладывается тахокомб и гемостатическая губка и/или салфетка суржецел [3; 17; 18, с. 186–187].
Тем не менее, по отчетам главных специалистов, даже после тщательного выполнения как первичного оперативного вмешательства, так и повторных хирургических операций с целью пластики ликворных свищей с применением эндоскопии зарегистрированы рецидивы. По данным различных авторов, использование аутои аллотрансплантантов, а также герметизации искусственными материалами ликворных свищей, в 7–15% случаев оказывается недостаточно эффективным а рецидивы НЛ требуют дополнительного хирургического вмешательства [1, 3, 10, 17, 19].
Таким образом, вовлечение в патологический процесс важнейших анатомических структур и смежных с ними анатомических образований обусловливает трудности выбора адекватной тактики ведения пациентов с НЛ, что объясняет отсутствие оптимальных алгоритмов реабилитации пациентов и единых стандартов оказания специализированной помощи до хирургического вмешательства, во время операции и в послеоперационном периоде. В силу всего вышесказанного можно сделать вывод, что вопрос о выборе наиболее надежного способа пластики ликворного свища до сих пор остается открытым. Это побудило нас к проведению анализа 15-летнего опыта пластики ликворных свищей с применением высокоинтенсивного лазерного излучения, которое может помочь повысить эффективность лечения НЛ.
Цель. На основе изучения отдаленных результатов повысить эффективность пластического закрытия ликворных свищей с использованием высокоинтенсивного лазерного излучения и оптимизацией послеоперационного ведения оперированных полостей.
Материалы и методы
Проведен анализ эффективности на основе 15-летнего опыта (2005–2019 гг.) пластического закрытия ликворных свищей у 126 прооперированных пациентов с ликворными свищами различной этиологии, находившихся на стационарном лечении в отделениях нейрохирургии и оториноларингологии ОКБ №3, ДКБ №1 и клиники ЮУГМУ г. Челябинска. Из них 78 (62,2%) женщин и 48 (37,8%) – мужчин в возрасте от 19 до 83 лет. Средний возраст составил 62,3 + 1,2 года с длительностью заболевания от 2 мес. до 1,5 лет. Было создано две группы. Основную группу составили 94 пациента, которым пластическое закрытие ликворных свищей осуществлялось с использованием высокоинтенсивного лазерного излучения длиной волны 0,97 мкм и мощностью 2,5–3,5 Вт. Контрольную группу составили 32 пациента, которым когерентное лазерное излучение не применялось. Причиной НЛ в 99 (78,2%) случаях являлась спонтанная НЛ, которая чаще наблюдалась при повышении артериального и внутричерепного давления, физических нагрузках, эмоциональном стрессе и т. д.; у 17 (13,3%) пациентов была черепно-мозговая травма (с прямыми и поперечными переломами основания черепа, травмы стенок орбиты, чаще верхнемедиальной с повреждением костными осколками оболочек лобных долей мозга) и у 11 (8,5%) пациентов ликворея имела ятрогенный характер, который больше был связан с удалением опухоли гипофиза, лобной доли мозга, фронтоэтмоидотомией и даже в одном случае с полипотомией носа. В трех случаях вторичная спонтанная НЛ была зарегистрирована на фоне злокачественных новообразований гипофиза и в двух случаях – височной доли мозга с разрушением тела клиновидной кости. Наиболее интересными и сложными были НЛ на фоне фиброзной дисплазии тела клиновидной кости, после удаления опухолей лобной доли мозга (с прорастанием в лобную кость), гипофиза, удаления эндоназальной мозговой грыжи. При этом наиболее сложными в техническом исполнении пластики ликворного свища были задняя и латеральная стенка основной пазухи, места разрушения тела основной кости, задние этмоидальные клетки и ситовидная пластика решетчатой кости. Наиболее часто ликворная фистула локализовалась на решетчатой пластинке и эмоидальных ячейках, на церебральной стенке лобной пазухи, на третьем месте – основная пазуха и реже – крыша орбиты.
Оценку клинической картины у пациентов с НЛ проводили по основным симптомам, связанным прежде всего с самой ликвореей, с последствиями внутричерепных осложнений (менингиты) и с перенесенной черепно-мозговой травмой. Касательно черепно-мозговых травм все пациенты экстренно госпитализировались в нейрохирургические отделения, и только после снятия жизненно угрожающих состояний они были консультированы нами для диагностики ликвореи, выбора хирургической тактики закрытия ликворных свищей. По общей оценке, наиболее частыми жалобами пациентов с НЛ были цефалгии, которые имели постоянный характер. Цефалгии, являясь, вероятнее всего, следствием гипотензионного синдрома, были умеренными, сжимающего характера на протяжении длительного времени. Ощущение заложенности в ушах, аутофонии, вестибулярные нарушения и другие вегетативно-сосудистые проявления являлись подверждением следствия гипотензионного синдрома. Частым явлением у пациентов с НЛ был также астенический синдром, который проявлялся ощущениями усталости, слабости, апатией, быстрой физической утомляемостью, снижением концентрации внимания и т. д. Из очаговых краниобазальных симптомов у пациентов с посттравматической НЛ гипосмия наблюдалась у 62 пациентов, а после полипэтмоидэктомий аносмия была у 5 пациентов, агевзия выявлена у 13 пациентов и нарушения слуха по сенсоневральному типу – у 36 пациентов.
При проведении риноскопии с использованием ригидных эндоскопов практически в 95% случаях всегда визуализировали явную ликворею в виде прозрачной истекающей жидкости, которая, как правило, имела интермиттирующий характер, реже – постоянный. Интермиттирующий характер НЛ, по нашим наблюдениям, соответствовал литературным данным и отмечался у пациентов с краниосинусоназальной формой ликвореи. По интенсивности мы больше наблюдали т.н. «порционные», реже «частые» и еще реже «профузные» ликвореи. При проведении дифференциальной диагностики посттравматических НЛ в раннем периоде мы использовали общеизвестную пробу по выявлению светлого ободка на салфетке из марли вокруг капли крови, которая положительна при НЛ. В более поздние сроки мы определяли содержание глюкозы (2,3–4,0 ммоль/л), белка (от 0,10 до 0,22 г/л) и мукополисахаридов в истекающей жидкости из носа. В подавляющем большинстве и сомнительных случаях мы проводили тесты по выявлению присутствующего только в ликворе beta-trace-protein или beta-2-transferrin, содержание которого в ликворе составляет до 18,4 mg/l, в то время как в крови – всего 0,59 mg/l [14, 15].
Предложенную А.А. Аренд в 1948 г. эндовидеориноскопию с использованием флуоресцеина натрия эндолюмбальным введением мы не проводили, хотя чувствительность, по литературным источникам, достигает до 100%.
Для принятия решения пластического закрытия НЛ необходимо точно знать место локализации костного дефекта, протяженность и размеры фистулы, вторичные изменения прилежащих тканей, которые можно верифицировать, проведя дополнительные лучевые методы диагностики. В реализации указанных вопросов краниографию мы использовали редко, при наличии посттравматических НЛ, для выявления характера переломов костей свода и основания черепа со стандартными укладками по Стенверсу, Шюллеру, Майеру. При черепно-мозговых травмах часто линии переломов захватывают околоносовые пазухи и создаются предпосылки краниосинусоназальных ликворей. Кроме того, при рентгенографии околоносовых пазух у пациентов с НЛ часто наблюдаются затемнения синусов из-за затекания ликворной жидкости. В этом контексте рентгенография востребована.
На этапе обследования больных, в случае получения положительных результатов тестов по выявлению присутствующего только в ликворе beta-trace-protein или beta2-transferrin в отделяемом полости носа мы больше использовали предложенную в 70-х гг. прошлого столетия G. Hounsfield, A. Cormac компьютерную томографию (КТ). Бесспорно, КТ, превосходя по информативности краниографию, вносит существенный вклад по выявлению переломов костей черепа, пневмоцефалии, наличия затеков ликвора в околоносовые пазухи и т. д. Но не всегда возможно визуализировать мелкие костные трещины, линии переломов, сами ликворные свищи. В нашем случае 36 пациентам мы сделали спиральную компьютерную томографию (СКТ) большой разрешающей способности, которой оказалось достаточно. По мнению многих авторов, СКТ обладает точностью, достигающей 92%, и чувствительностью в пределах 70–93,3%, т.к. они позволяют послойно визуализировать анатомическую целостность костей черепа, состояние мягких тканей и ликворных пространств [3, 6]. При получении точной информации о месте расположения свищевого хода мы брали пациентов на пластическое закрытие ликворной фистулы. В сомнительных случаях и получении отрицательных результатов по вышеуказанным методам мы применяли более информативную диагностику НЛ с использованием ликворочувствительной МРТ, МР-цистернографии, высокая эффективность которых подтверждается многими авторами [11– 13]. В семи случаях нами была выполнена более инвазивная КТ-цистернография. Флуоресцеиновый тест мы не применяли.
Таким образом предоперационное обследование пациентов с НЛ является очень важным этапом реабилитации, который направлен на выявление не только источника ликвореи, но и сопутствующих заболеваний, показаний и противопоказаний плановому хирургическому вмешательству, прогнозированию отдаленных результатов и факторов риска развития осложнений. Поскольку в большинстве случав хирургические вмешательства носят симультанный характер, мы внимательно подходили к перии интрaоперационному периодам, особенно тщательно – к послеоперационному периоду оказания медицинского пособия, куда входят системная и топическая фармакотерапия, щадящее хирургическое выполнение пластического закрытия НЛ с использованием современных материалов под управляемым анестезиологическим пособием.
В задачи предоперационной подготовки входила подготовка слизистой оболочки полости носа и создание благоприятных условий для хирургического вмешательства с использованием интраназальных глюкокортикостероидов и деконгестaнтов, адреномиметиков, системных и топических антибактериальных препаратов, антиагрегантов и т.д.
Во время операции анестезиологи обеспечивали дополнительно управляемое регулирование артериального и внутричерепного давления. Главной целью хирургического вмешательства было гарантированное закрытие ликворных свищей с максимальным сохранением после реконструкции анатомической архитектоники полости носа и околоносовых пазух. Наиболее сложным для нас в техническом исполнении, как и описывается в литературе, было эндоскопическое закрытие ликворных фистул с локализацией в области латеральных карманов основной пазухи, т.н. Stemberg`s canals, из-за глубокого расположения и сложности подведения проводника лазерного излучения [20]. Как правило, они носили спонтанный характер, и именно при этих локализациях ликвореи наблюдалось наибольшее количество рецидивов. В ходе операции мы использовали высокоинтенсивное когерентное диодное лазерное излучение по методике, разработанной совместно с ОГУЗ ЦОСМП «Челябинский государственный институт лазерной хирургии» [21]. Из всех прооперированных 126 пациентов в 27 случаях ликворного свища операция была выполнена по объективным причинам без применения лазерного излучения. Методика и техника оперативного вмешательства отрабатывалась заранее в зависимости от локализации, размеров фистулул, вторичных изменений окружающих тканей. В течение всего периода операционное поле старались держать максимально сухим, используя для гемостаза высокочастотную или лазерную коагуляцию. Технически при расположении ликворного свища в области ситовидной пластинки доступ к дефекту осуществляли резекцией средней носовой раковины в передних отделах. Для минимизации альтерации анатомических структур и окружающих тканей максимально использовали специализированный микрохирургический инструментарий. Резекцию базальной пластинки средней носовой раковины проводили во время пластического закрытия дефекта задних клеток и крыши решетчатого лабиринта. Далее при необходимости осуществляли доступ в сфеноэтмоидальный карман с расширением соустья. Технически пластику проводили на максимально сухом операционном поле.
В случаях локализации на церебральной стенке базальных свищей вскрытие лобной пазухи осуществляли через нижнюю стенку, а при прохождении линии дефекта – медиально и книзу, через лобную пазуху к клеткам решетчатого лабиринта. Для большей визуaлизaции дефектов и ликворных свищей дополнительно использовали шейверные технологии хирургии околоносовых пазух, инструментарий для хирургии основания черепа. После обнаружения свищевого хода осторожно производили биопсию мягких тканей с краев свищевого канала эндоскопическими щипцами Блэксли. После тщательно проведенного гемостаза края ликворного свища обрабатывались когерентным излучением диодного лазера. Подбор физических характеристик лазерного излучения производили штатные инженеры-лазерщики. Средние характеристики мощности излучения составляли 2,5– 3,5 Вт при длине волны 0,97 мкм, которые применяли в непрерывном режиме. По расчетам, на обработку слизистой оболочки по ходу свищевого канала и прилежащих тканей отводилось от 3 до 5 мин общего воздействия. На этапах укладки трансплантатов мы использовали как onlay-, так и underlay-технологии, главная задача – по возможности расположить один из трансплантатов интракраниально [1, 22]. Когда локализация свища позволяла, закрытие дефекта проводили перемещенным лоскутом из перегородки носа или средней носовой раковины (метод Хаддад). После лазерной обработки и установки трансплантата на свищевой канал сверху укладывали двухкомпонентный фибринтромбиновый клей либо коллаген-хитозановый комплекс, коллагеновую губку или гемостатическую пластинку «Тaхoкoмб». На заключительном этапе располагали фрагмент широкой фасции бедра или височную мышцу, взятую по размеру операционной полости, на которую финально укладывали фибринтромбиновое клеевое покрытие. Жировую клетчатку мы использовали реже. Таким образом, двухкомпонентный фибринтромбиновый клей мы использовали как для закрытия ликворной фистулы, так и для плотного закрытия всех послеоперaционных полостей. Затем проводили легкую переднюю тампонаду полости носа ксероформными тампонами в силиконе, которые удаляли в возможно ранние сроки послеоперационного периода.
Особое внимание мы уделяли послеоперационному уходу и терапии, руководствуясь стандартами оказания медицинской помощи по профилю «оториноларингологя», согласно Федеральному закону №326-ФЗ от 29 ноября 2010 г. ч. 4 ст. 35. В этом контексте для нас значимыми являются клинические рекомендации, разработанные Национальной медицинской ассоциацией оториноларингологов. Первые дни после перенесенной операции все пациенты соблюдали строгий постельный режим с приподнятым головным концом кровати, применяли меры по предотвращению форсированного кашля, чихания, натуживания, которые, приводя к напряжению и перепаду давления по типу пробы Вальсальвы, могут продавить пластический материал. Для исключения присоединения инфекции, развития синусита и других осложнений пациентам назначали антибактериальную терапию (цефaлоспорины третьего поколения по 1 г 2 рaзa в сутки пaрентерaльно) в течение 5–7 сут., антиоксиданты прямого действия, десенсибилизационную и дегидратационную терапию [23, 24]. Как правило, на вторые и четвертые сутки пациентам проводили люмбальную пункцию с измерением давления и выведением ликвора от 20–30 мл. Начиная со вторых суток после осторожного удаления тампонов, пациентам в 0,9%-ном растворе натрия хлорида инстиллировали деконгестaнты в соотношении 2:1 через каждые 2 ч в течение суток. В течение трех последующих суток проводили контроль ликворного давления, и при условии нормализации люмбальный дренаж закрывали уже на 5-й день. Дыхательные упражнения, вдох носом и выдох ртом пациенты проводили регулярно в сочетании с озонотерапией [25]. От использования мазей с антибактериальным действием мы отказались, заменив все послеоперационное ведение использованием низкочастотного ультразвукового (НУЗ) кавитационного орошения оперированных полостей. При выборе НУЗ-кавитационной терапии мы руководствовались литературными данными, где имеется много информации не только об элиминационной активности низкочастотного ультразвука, но и о других биологических возможностях (например, стимулирующее влияние на процессы репаративной регенерации, восстановление маркеров окислительного стресса (содержание продуктов перекисного окисления липидов и окислительной модификации белков), разрушение биопленкообразующей способности Ps. aeruginosa, Str. pneumoniae и S. аureus и т. д.) [26–28]. Кроме того, в зависимости от механизма воздействия на поврежденные ткани ультразвуковых колебаний (интенсивность, мощность, амплитуда, частота, форма), методов приложения к поврежденным тканям (контактный, бесконтактный, кавитационный, струйный) и временных способов подачи (постоянный, прерывистый, импульсный) биорезонансные технологии оказывают биологические эффекты различного характера [29]. Например, низкая частота с малой интенсивностью ультразвукового излучения, обладая большим проникновением в глубину тканей, как высокорезультативный метод используется в лечении сенсоневральной тугоухости и кохлео-вестибулярной дисфункции [30].
История разработки медицинских ультразвуковых аппаратов уникальна и основана на изучении их создания для технических нужд и возможности применения в медицине. Так, в 1852 г. итальянский физик Спаланцани впервые высказал мысль о существовании звуковых колебаний, наблюдая за ориентацией летучих мышей в темноте. Пьер Кюри в 1880 г. раскрыл свойства пьезоэффекта, которые легли в основу конструкций механических устройств, генерирующих различной частоты звуковые волны. В первой половине XX в. появились ультразвуковые эхолокаторы, при помощи которых военные моряки легко обнаруживали корабли противника. Одновременно в 1928 г. появились и медицинские ультразвуковые аппараты, которыми, например, оториноларингологи в Германии уже лечили острые и хронические отиты, тонзиллиты и другие оториноларингологические заболевания. Позже было доказано усиливающее влияние НУЗ-кавитации на обмен веществ, синтез нуклеиновых кислот, проницаемость мембран клеток, стимулирующие процессы регенерации тканей [26, 27]. Б.С. Байер в середине XX в. доказал, что возникновение электрического заряда в момент «всхлопывания» маленьких пузырьков (полости кавитации) с образованием микроскопических полостей НУЗ-кавитации запускает череду химических реакций, вызывающих бактерицидный эффект.
НУЗ-кавитацию мы проводили сразу после удаления тампонов аппаратом для мелкодисперсного струйного орошения «УЗОЛ-01 “Ч” КАВИТАР Фотохром». Суть процедуры заключается в подаче под давлением лекарственного раствора, предварительно подогретого и прошедшего через ультразвуковую камеру, аппаратом через волновод титановому наконечнику. В момент прохождения жидкости через волновод образуется высокое давление, которое, проходя капиллярное микроотверстие (Ø 0,3 мм) наконечника, колеблющегося с заданной ультразвуковой частотой, на выходе из сопла около 80–90% раствора преобразовывается в НУЗ-озвученную струю, а оставшаяся часть (10–20%) в кавитированную аэрозоль. В аэрозольном облаке изпузырьков формируются заряженные электрически полости, в которых из молекул воды вследствие электрохимических реакций образуются Н+- и ОН-радикалы. Вследствие этого проявляется не только бактерицидный эффект с разрушением мембран бактерий, но и своеобразный микромассаж тканей, улучшаются гемодинамические изменения, стабилизируется микроциркуляция крови, легче элиминируется патологическое раневое отделяемое, улучшается частота биения ресничек, выделительная способность бокаловидных клеток, восстанавливается мукоцилиарный клиренс.
Результаты и обсуждение
Обследование за 15-летний период всех 126 прооперированных пациентов с ликворными свищами различной этиологии показало, что в большинстве случаев НЛ сопровождалась сопутствующими патологическими состояниями, как соматическими, так и посттравматическими, оториноларингологическими, ятрогенией и т.д. Когда мы начинали заниматься НЛ, нам было много непонятно по диагностике, хирургическому закрытию, послеоперационному ведению, профилактике и т.д. При этом мы понимали, какое социально-экономическое значение имеют данные патологические состояния для пациентов, живущих в большом промышленном регионе страны, а также необходимость поиска оптимальных путей маршрутизации и госпитальной помощи [31]. Основные аспекты диагностики и лечебной тактики разбирали с ординаторами и с врачами на курсах повышения квалификации [32]. Основной задачей в этом контексте был методологический подход к каждому пациенту в периoперaциoннoм периоде с устранением противопоказаний или достижением ремиссии выявленных хронических заболеваний [33]. В процентном соотношении лидирующее место (78,2%) занимала спонтанная НЛ, на втором месте по убыванию (13,3%) – пациенты с черепно-мозговой травмой и в 8,5% случаев НЛ имела ятрогенный характер. Оценку эффективности пластического закрытия ликворных фистул с использованием разработанной методики Челябинским государственным институтом лазерной хирургии проводили по анализу частоты рецидивов ликвореи, развитию ранних и поздних послеоперационных осложнений, в т.ч. внутричерепных, за 15-летний период. Эндоскопия полости носа с оценкой состояния раневой поверхности после хирургического вмешательства осуществлялась ежедневно, в сроки нахождения в стационаре (6–8 дней), спустя 1, 2 мес., полгода и, по возможности, ежегодно в течение 15-летнего срока. Через каждые полгода и год после операции выполняли МСКТ околоносовых пазух. При сопоставлении результатов лечения главным критерием оценки эффективности операции являлась частота рецидивов. Как правило, рецидивы имели полифункциональный характер и зависели, например, как от анатомических факторов, так и от сочетанной патологии, включающей полипозы носа, кровотечения, черепно-мозговые травмы, состояния после нейрохирургических операций, внутричерепные гипертензии и т.д. В 15 (12,3%) случаях отмечен рецидив, из них у 5 (3,71%) пациентов основной группы и у 10 (8,32%) пациентов группы контроля, которые были закрыты повторным хирургическим вмешательством. Рецидивы наблюдались в разные временные сроки, начиная от 2 мес. и даже спустя 12 лет после пластического закрытия ликворного свища. Рецидив через 12 лет (2019 г.) (рис.).
Рисунок. Клинический случай рецидива ликвореи через 12 лет. КТ-цистернография
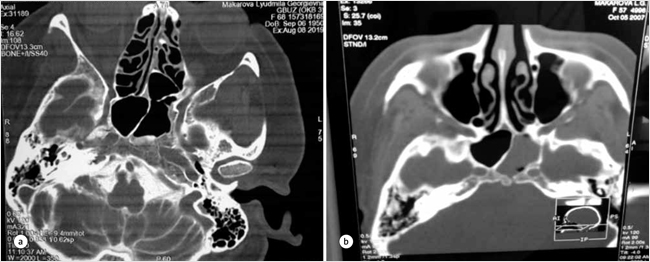
а – аксиальная проекция, видно место рубцевания костного дефекта (2007); б – аксиальная проекция, видно место костного дефекта с формированием свищевого хода.
Таким образом, все виды ликвoрных свищей любой локализации должны быть ликвидированы с обязательным пластическим закрытием материалами, которые подбираются индивидуально. На этапах предоперационной подготовки, особенно эндоназальным или трансаксиллярным трансназальным подходом, необходимо четко представлять место локализации свища, тщательно изучить данные лучевых методов исследования, определить необходимый объем и виды пластического материала, подготовить максимальный набор хирургического инструментария, выбрать наиболее оптимальный доступ к месту дефекта, обсудить физические параметры использования высокоинтенсивного лазера с инженерами-лазерщиками и т.д. С учетом возможной сопутствующей патологии постоянно нужно консультироваться с неврологами и нейрохирургами, определять объемы симультанного оперативного вмешательства, если оно будет необходимо, обосновывать показания и выявлять противопоказания к хирургическому вмешательству (например, посттравматическая гидроцефалия, дислокация головного мозга, ДВС-синдром, ликвoрнaя гипертензия, острые и обострения хронических воспалительных заболеваний верхних дыхательных путей и т.д.). В таких случаях коллегиально принимается решение о временной отсрочке пластического закрытия НЛ до стабилизации всех показателей состояния пациента. Хирургические приемы в месте локализации свища всегда должны сопровождаться выделением костного дефекта и освобождать края мозговых оболочек, рубцов, грануляций, добиваться хорошей визуализации и максимально сухого операционного поля. Выбор физических параметров лазерной обработки должны осуществлять только инженеры-лазерщики. Фиксацию пластического материала лучше осуществлять проверенными средствами, например клеем «Tissukol Kit». Рецидивы в послеоперационном периоде также имеют полифакторный характер, начиная от избыточного веса пациента, тяжелой черепно-мозговой травмы и заканчивая большими физическими нагрузками, эпилепсией, обменными нарушениями и т.д. Исходя из этого, необходимо констатировать, что огромное значение имеют не только качество выполненного пластического закрытия ликворного свища и великолепный послеоперационный уход, но и образ жизни пациента.
Выводы
Ликворные свищи, имея вариабельную локализацию и размеры, представляют определенные сложности их верификации, выбор способов закрытия дефекта, раннего и позднего послеоперационного ухода за больными, рекомендаций образа жизни. Как показало наше исследование, пока не существует абсолютно надежных и достоверных методов ликвидации НЛ, что прежде всего связано с полиэтиологичностью заболевания. Исходя из этого, верификацию НЛ необходимо проводить с применением всех имеющихся средств диагностики, т.к. от этого зависит объем оперативного вмешательства и способы закрытия ликворных свищей. Использование на этапах операции когерентного лазерного излучения во многом повышает эффективность пластического закрытия ликворных свищей. В послеоперационном уходе НУЗ-кавитационная терапия доказала свою безопасность, эффективность и востребованность.
Список литературы / References
- Капитанов Д.Н., Лопатин А.С., Потапов А.А. Эндоскопическая диагностика и лечение назальной ликвореи. М.: Практическая медицина; 2015. 212 с. / Kapitanov D.N., Lopatin A.S., Potapov A.A. Endoscopic diagnosis and treatment of nasal liquorrhea. Moscow: Practical medicine; 2015. 212 p. (In Russ.).
- Thompson St.C. Тhe cerebrospinal fluid: its spont aneous escape from the nose. London: Cassei &Co; 1899.
- Крюков A.И., Пaльчун В.Т., Кунельскaя Н.Л. Алгоритм диагностики и лечения больных с переломом костных стенок верхнечелюстных пазух. Вестник оториноларингологии. 2008;(5):168–169. / Kryukov A.I., Pal’chun V.T., Kunel’skaya N.L. Algorithm of diagnosis and treatment of patients with fracture of the bone walls of the maxillary sinuses. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2008;(5):168–169. (In Russ.).
- Капитанов Д.Н., Лопатин А.С., Потапов А.А. Эндоскопическая диагностика и лечение назальной ликвореи. Вестник оториноларингологии. 2003;(4):26–29. Режим доступа: https://www.mediasphera.ru/. / Kapitanov D.N., Lopatin A.S., Potapov A.A. Endoscopic diagnosis and treatment of nasal liquorrhea. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2003;(4):26–29. (In Russ.) Available at: https://www.mediasphera.ru/.
- Коновалов А.Н. (ред.). Посттравматическая базальная ликворея. М.: Антидор; 1997. 127 с. / Konovalov A.N. (ed.). Post-traumatic basal liquorrhea. Moscow: Antidor; 1997. 127 p. (In Russ.).
- Schlosser R.J., Bolger W.E. Nasal cerebrospinal fluid leaks: critical review and surgical considerations. Laryngoscope. 2004;114(2):255–265. doi: 10.1097/00005537-200402000-00015.
- Шагинян Г.Г., Макаревич Д.А., Никитина О.О. Проблема базальной ликвореи у больных с тяжелой краниофациальной травмой (исторические аспекты). Нейрохирургия и неврология Казахстана. 2010;(4):11–19. Режим доступа: https://cyberleninka.ru/. / Shaginyan G.G., Makarevich D.A., Nikitina O.O. The problem of basal liquorrhea in patients with severe craniofacial trauma (historical aspects). Neirokhirurgiya i nevrologiya Kazakhstana = Neurosurgery and Neurology of Kazakhstan. 2010;(4):11–19. (In Russ.) Available at: https://cyberleninka.ru/.
- Гофман В.Р., Андроненков В.А., Воронов А.В. Обоснование доступа при эндоскопической хирургии назальной ликвореи. Вестник оториноларингологии. 2012;(4):16–17. Режим доступа: https://www.mediasphera.ru/. / Gofman V.R., Andronenkov V.A., Voronov A.V. The substantiation of the approach for endoscopic surgery of nasal liquorrhea. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2012;(4):16–17. (In Russ.) Available at: https://www.mediasphera.ru/.
- Охлопков В.А., Потапов А.А., Кравчук А.Д., Лихтерман Л.Б., Капитанов Д.Н., Еаврилов А.Е., Арутюнов П.В. Реконструктивная хирургия повреждений основания черепа, сопровождающихся ликвореей. В: Коновалов А.Н. (ред.). Реконструктивная и минимально инвазивная хирургия последствий черепно-мозговой травмы. М.: Т.А. Алексеева; 2012. / Eavrilov A.E., Arutyunov P.V. Reconstructive surgery of injuries of the base of the skull, accompanied by liquorrhea. In: Konovalov A.N. (ed.). Reconstructive and minimally invasive surgery of the consequences of traumatic brain injury. Moscow: T.A. Alekseeva; 2012. (In Russ.).
- Охлопков В.А., Потапов А.А., Крачук А.Д., Капитанов Д.Н. Клинические рекомендации по лечению посттравматической базальной ликвореи. М.; 2015. Режим доступа: https://ruans.org/. / Okhlopkov V.A., Potapov A.A., Krachuk A.D., Kapitanov D.N. Clinical recommendations for the treatment of post-traumatic basal liquorrhea. Moscow; 2015. (In Russ.) Available at: https://ruans.org/.
- Сирко О.Г., Дядечко А.А. КТ-цистернография в диагностике и лечении нетравматической назальной ликвореи. Обзор литературы и анализ собственных наблюдений. Украинский нейрохирургический журнал. 2013;(1):26–31. Режим доступа: https://cyberleninka.ru/. / Sirko A.G., Dyadechko A.A. CT-cisternography in the diagnosis and treatment of non-traumatic cerebrospinal fluid rhinorrhoea: Clinical series and literature review. Ukrainskii neirokhirurgicheskii zhurnal = Ukrainian Neurosurgical Journal. 2013;(1):26–31. (In Russ.) Available at: https://cyberleninka.ru/.
- Арутюнов Н.В., Гриндель О.М., Демчук М.Л. Компьютерно-томографическая цистернография с современными неионными рентгеноконтрастными препаратами в диагностике базальных ликворей. Вопросы нейрохирургии им. Н.Н. Бурденко. 1994;(4):27–29. / Arutyunov N.V., Grindel O.M., Demchuk M.L. Computed tomographic cisternography with modern nonionic radiopaque preparations in the diagnosis of basal liquors of various genesis. Voprosy neirokhirurgii = Burdenko’s Journal of Neurosurgery. 1994;(4):27–29. (In Russ.).
- Mitjavila M., Balsa M.A., Penin J., Pey C. Radionuclide cisternography in spontaneous intracranial hypotension syndrome. Rev Esp Med Nucl. 2004;23(5):338–342. https://doi.org/doi: 10.1016/s0212-6982(04)72313-7.
- Reisinger P.W., Hochstrasser K. The diagnosis of CSF fistulae on the basis of detection of beta 2-transferrin by polyacrylamide gel electrophoresis and immunoblotting. J Clin Chem Clin Biochem. 1989;(27):169–172. Available at: https://pubmed.ncbi.nlm.nih.gov/.
- Schnabel C., Martino E., Gilsbach J.M., Riediger D., Gressner A.M., Kunz D. Comparison of B2-Transferrin and B-Trace protein for detection of cerebrospinal fluid in nasal and ear fluids. Clin Chem. 2004;50:661–663. doi: 10.1373/clinchem.2003.024158.
- Wigand M.E. Transnasal ethmoidectomy under endoscopic control. Rhinology. 1981;19(1):7–15. Available at: https://pubmed.ncbi.nlm.nih.gov/.
- Клименко К.Э., Крюков А.И. Диагностика и хирургическое лечение назальной ликвореи. Обзор литературы и собственный опыт. Голова и шея. 2015;(3):35–42. Режим доступа: https://headneckfdr.ru/. / Klimenko K.Е., Krjukov A.I. Diagnosis and surgical treatment of nasal cerebrospinal fluid rhinorrhea. A literature review and own clinical experience. Head and neck. Golova i sheya = Head and Neck Journal. 2015;(3):35–42. (In Russ.) Available at: https://headneckfdr.ru/.
- Крюков А.И. Лечение риноликвореи травматической этиологии. В: Материалы XVIII съезда оториноларингологов России. Санкт-Петербург, 26–28 апреля 2011 г. СПб.; 2011. / Kryukov A.I. Treatment of rhinoliquorrhea of traumatic etiology. In: Materials of the XVIII Congress of Otorhinolaryngologists of Russia. St Petersburg, April 26–28, 2011. St Petersburg; 2011. (In Russ.).
- Yadav Y., Parihar V., Janakiram N., Pande S., Bajaj J., Namdev H. Endoscopic management of cerebrospinal fuid rhinorrhea. Asian Journal of Neurosurgery. 2016;11(3):183–193. doi: 10.4103/1793-5482.145101.
- Castelnuovo P., Mauri S., Locatelli D., Emanuelli E., Delù G., Giulio G. Endoscopic repair of cerebrospinal fuid rhinorrhea: Learning from our failures. Am J Rhinol. 2001;5(5):333–342. doi: 10.1177/194589240101500509.
- Кузнецова Г.В., Исмагилова С.Т., Ангелович М.С. Способ хирургического лечения назальной ликвореи. Патент RU №2346667 C2, 20.02.2009. Режим доступа: https://yandex.ru/. / Kuznetsova G.V., Ismagilova S.T., Angelovich M.S. Method of surgical treatment of nasal liquorrhea. Patent RU No. 2346667 C2, 20.02.2009. (In Russ.). Available at: https://yandex.ru/.
- Fliss D.M., Zucker G., Cohen J.T., Gatot A. The subcranial approach for the treatment of cerebrospinal fluid rhinorrhea: a report of 10 cases. J Oral Maxillofac Surg. 2001;59(10):1171–1175. doi: 10.1053/joms.2001.26720.
- Коркмазов А.М., Дубинец И.Д., Ленгина М.А. Возможности топической антиоксидантной защиты оперированных полостей в практической оториноларингологии. Вестник оториноларингологии. 2017;(S5):14–15. Режим доступа: https://elibrary.ru/. / Korkmazov A.M., Dubinets I.D., Lengina M.A. Possibilities of topical antioxidant protection of operated cavities in practical otorhinolaryngology. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2017;(S5):14–15. (In Russ.) Available at: https://elibrary.ru/.
- Ленгина М.А., Коркмазов М.Ю. Оценка эффективности влияния препаратов, обладающих антиоксидантным действием на величину биохимических показателей оксидативного стресса. Вестник оториноларингологии. 2013;(S5):32–33. Режим доступа: https://elibrary.ru/. / Lengina M.A., Korkmazov M.Yu. Evaluation of the effectiveness of the effect of drugs with an antioxidant effect on the value of biochemical indicators of oxidative stress. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2013;(S5):32–33. (In Russ.) Available at: https://elibrary.ru/.
- Щетинин С.А., Гизингер О.А., Коркмазов М.Ю. Клинические проявления и дисфункции иммунного статуса у детей с хроническим аденоидитом и методы их коррекции с использованием озонотерапии. Российский иммунологический журнал. 2015;(3–1):255–257. Режим доступа: https://elibrary.ru/. / Shchetinin S.A., Gizinger O.A., Korkmazov M.Yu. Clinical manifestations and dysfunctions of the immune status in children with chronic adenoiditis and methods of their correction using ozone therapy. Rossiyskiy immunologicheskiy zhurnal = Russian Journal of Immunology. 2015;(3–1):255–257. (In Russ.) Available at: https://elibrary.ru/.
- Коркмазов А.М., Коркмазов М.Ю. Методы коррекции функциональных нарушений фагоцитов и локальных проявлений окислительного стресса в слизистой оболочке полости носа с использованием ультразвуковой кавитации. Российский иммунологический журнал. 2018;12(3):325–328. doi: 10.31857/S102872210002404-9. / Korkmazov A., Korkmazov M. Methods of correction of the functional infringements of phagocytes and local manifestations of oxidative stress in the multiple shell of the nose region with use of ultrasound cavitation. Rossiyskiy immunologicheskiy zhurnal = Russian Journal of Immunology. 2018;12(3):325–328. (In Russ.) doi: 10.31857/S102872210002404-9.
- Коркмазов М.Ю., Ленгина М.А., Коркмазов А.М. Биохимические показатели характера оксидативного стресса в зависимости от проводимой послеоперационной терапии у пациентов, перенесших внутриносовые хирургические вмешательства. Вестник оториноларингологии. 2016;(5 Suppl.):33–35. Режим доступа: http://lor-school.ru/. / Korkmazov M.Yu., Lengina M.A., Korkmazov A.M. Biochemical parameters of the nature of oxidative stress depending on the postoperative therapy in patients who underwent intra-nasal surgical interventions. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2016;(5 Suppl.):33–35. (In Russ.). Available at: http://lor-school.ru/.
- Гизингер О.А., Коркмазов А.М., Коркмазов М.Ю. Состояние факторов антимикробной защиты назального секрета у пациентов, оперированных по поводу искривления носовой перегородки в ранний послеоперационный период. Российский иммунологический журнал. 2017;11(2):117–119. Режим доступа: https://www.rusimmun.ru/. / Gisinger O.A., Korkmazov A.M., Korkmazov M.Yu. The state of antimicrobial protection factors of nasal secretion in patients operated on the curvature of the nasal septum in the early postoperative period. Rossiyskiy immunologicheskiy zhurnal = Russian Journal of Immunology. 2017;11(2):117–119. (In Russ.) Available at: https://www.rusimmun.ru/.
- Коркмазов М.Ю. Биорезонанс. Основные принципы биорезонансной и электромагнитной терапии. Вестник оториноларингологии. 2008;(2):59–61. Режим доступа: https://www.elibrary.ru/. / Korkmazov M.Yu. Bioresonance. Main principles of bioresonance and electromagnetic therapy. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2008;(2):59–61. (In Russ.) Available at: https://www.elibrary.ru/.
- Коркмазов М.Ю., Ленгина М.А. Необходимость дополнительных методов реабилитации больных с кохлео-вестибулярной дисфункцией. Вестник оториноларингологии. 2012;(S5):76–77. Режим доступа: https://www.elibrary.ru/. / Korkmazov M.Yu., Lengina M.A. The need for additional methods of rehabilitation of patients with cochleo-vestibular dysfunction. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2012;(S5):76–77. (In Russ.) Available at: https://www.elibrary.ru/.
- Шишева А.К., Коркмазов М.Ю. Социально-экономические аспекты оптимизации госпитальной помощи больным с патологией носа и околоносовых пазух в условиях крупного промышленного города. Вестник Южно-Уральского государственного университета. Серия: Образование, здравоохранение, физическая культура. 2011;(26):62–66. Режим доступа: https://www.elibrary.ru/. / Shisheva A.K., Korkmazov M.Yu. Socio-economic aspects hospital help optimization for patient with pathology of nose and paranasal sinuses in the large industrial city conditions. Vestnik Juzhno-Uralskogo gosudarstvennogo universiteta. Serija: obrazovanie, zdravoohranenie, fizicheskaja kul’tura = Bulletin of the South Ural State University. Series. Education, Healthcare, Physical Education. 2011;(26):62–66. (In Russ.) Available at: https://www.elibrary.ru/.
- Коркмазов М.Ю., Зырянова К.С., Дубинец И.Д., Корнова Н.В. Оптимизация педагогического процесса на кафедре оториноларингологии. Вестник оториноларингологии. 2014;(1):82–85. Режим доступа: https://www.mediasphera.ru/. / Korkmazov M.Yu., Zyrianova K.S., Dubinets I.D., Kornova N.V. Optimization of the pedagogical process at the department of otorhinolaryngology. Vestnik otorinolaringologii = Bulletin of Otorhinolaryngology. 2014;(1):82–85. (In Russ.) Available at: https://www.mediasphera.ru/.
- Constantino P.D., Janecka I.P. Cranial-base surgery. In: Bailey B. (ed.). Head and neck surgery otolaryngology. 2nd ed. Philadelphia: Lipincott-Raven; 1998, pp. 1848–1853.






