
Журнал "Медицинский совет" №8 2018
В.М. Свистушкин, д.м.н., профессор, С.В. Старостина, д.м.н., профессор, О.И. Баум, д.ф-м.н., Л.В. Селезнева, А.В. Старостин Первый Московский государственный медицинский университет им. И.М. Сеченова Минздрава России (Сеченовский университет)
В статье представлен новый метод пластики дефекта гортани и трахеи, основанный на экспериментальных исследованиях, который позволит восстановить анатомическую целостность дыхательных путей на заключительном этапе хирургического лечения. Представлено собственное клиническое наблюдение.
V.M. SVISTUSHKIN, MD, Prof., S.V. STAROSTINA, MD, Prof., O.I. BAUM, MD in physics and mathematics, L.V. SELEZNEVA,A.V. STAROSTIN I.M.Sechenov First Moscow State Medical University of the Ministry of Health of Russia (Sechenov University)
THE LASER MODELING OF COSTAL AUTOCARTILAGE IN LARYNGOTRACHEOPLASTY. THE CLINICAL CASE
This article presents the new method of plastics of larynx and trachea defect. The method is based on expiremental research
and it will allow to restore an anatomical integrity of airways at the final stage of surgical treatment. Personal clinical
observation is presented.
Опыт хирургического лечения больных с обширными ларинготрахеальными дефектами показывает, что, несмотря на многочисленность экспериментальных работ и попыток клинических решений, до сих пор не найдены оптимальные методики пластики ларинготрахеостом [1].
На сегодняшний день существует множество способов пластики дефектов передней стенки гортани и трахеи с применением биологических ауто- и аллотрансплантатов (хрящи, мышцы, кожные лоскуты) [2, 3] и искусственных материалов (никелид титана [4], марлекс [5], силикон, танталовые и капроновые сетки и др. [6–8], которые не всегда отвечают необходимым требованиям пластики по своим биоинертным свойствам и неспособности восстанавливать форму полых органов шеи и подвергаются лизису.
В клинике болезней уха горла и носа Первого МГМУ им. И.М. Сеченова впервые экспериментально доказана возможность моделирования реберного аутохряща волоконным эрбиевым лазером на 10 лабораторных кроликах породы шиншилла. Стабильность полученных имплантированных кроликам хрящей исследовалась в течение трех месяцев, после чего производилась аутопсия изучаемого фрагмента реберного хряща и его патоморфологическое исследование. По данным гистологического исследования в микропрепаратах отмечалось наличие многочисленных лакун с незрелыми хондроцитами, что свидетельствовало о росте молодой хрящевой ткани [9].
В исследовании было показано, что в условиях физиологической среды новая смоделированная Er-лазером форма хряща является стабильной и не претерпевает изменений со временем, что позволило разработать и обосновать способ применения излучения Er (эрбиевого) лазера в лечении больных с хроническими рубцовопаралитическими стенозами гортани и трахеи на заключительном этапе хирургического лечения.
В клинике болезней уха, горла и носа Университетской клинической больницы №1 ПМГМУ им. И.М. Сеченова впервые проведено хирургическое лечение больной с обширным ларинготрахеальным дефектом с использованием в качестве пластического материала моделированного волоконным лазером реберного аутохряща.
Больная К., 31 год, обратилась в Клинику болезней уха, горла и носа Первого МГМУ им. Сеченова в феврале 2016 г. с жалобами на невозможность дыхания через естественные пути, наличие трахеостомической трубки.
Из анамнеза известно, что больная перенесла струмэктомию по поводу узлового зоба щитовидной железы в июле 2014 г., после чего через месяц стала отмечать затруднение дыхания через естественные пути. В течение последующих 6 месяцев одышка при минимальной физической нагрузке нарастала. В 2015 г. при обследовании по месту жительства по данным непрямой ларингоскопии был диагностирован двусторонний паралич и декомпенсированный стеноз гортани: выполнена нижняя трахеостомия.
При осмотре – дыхание через трахеостомическую трубку свободное, трахеостома расположена сразу под дугой перстневидного хряща. Форма шеи правильная, симптом Мура положительный. По данным непрямой ларингоскопии и ларингостробоскопии: слизистая оболочка гортани розовая, надгортанник развернут в форме лепестка, грушевидные синусы свободные, голосовые складки в срединном положении, при дыхании и фонации неподвижны, ширина голосовой щели на вдохе 1 мм. Подголосовое пространство не обозримо. Отмечается охриплость голоса.
25.02.2016 г. в нашей клиникебыло проведено хирургическое лечение в объеме открытой ларинготрахеопластики с экстраларингеальной латерофиксацией правой голосовой складки и аритенохордотомией справа и эндопротезированием Т-образной трубкой. Срок стентирования силиконовой Т-образной трубкой в послеоперационном периоде составил 8 месяцев. Контрольный период после деканюляции продолжался 2 месяца.
С целью проведения заключительного этапа хирургического лечения – пластического закрытия ларинготрахеального дефекта в феврале 2017 г. больная повторно госпитализирована с клиническим диагнозом «Хронический паралитический стеноз гортани». Состояние после струмэктомии (2014), трахеостомии (2015), ларинготрахеопластики с экстраларингеальной латерофиксацией правой голосовой складки, аритенохордотомией справа и эндопротезированием Т-образной трубкой (2016). Ларинготрахеальный дефект.

Ход оперативного лечения:
1. Подготовка каркасного материала для пластического закрытия дефекта гортани и трахеи с применением моделированного аутохряща с помощью высокоэнергетического лазерного воздействия: Первым этапом производился забор реберного хряща пациента. При резекции хрящевой части реберной дуги формировались три полоски толщиной до 0,5 см, длиной 3 см, шириной до 1,5 см. Производилось моделирование одного из полученных хрящевых фрагментов лучом эрбиевого волоконного лазера длиной волны 1,56 мкм (излучение доставляется опто-термо-механическим контактором, время облучения
каждой точки 6 сек., мощность 2,2 Вт) до получения стабильной полукруглой формы.
28.02.2017 г. был выполнен заключительный этап хирургического лечения: пластика ларинготрахеального дефекта моделированным эрбиевым лазером – реберным аутохрящем (заявка на изобретение в Роспатент №2017126119 от 20.07.2017).

В ближайшем послеоперационном периоде фиброларингоскопическая картина: слизистая оболочка гортани розовая; голосовые складки серого цвета, правая – в латеропозиции, левая – в срединном положении; ширина голосовой щели 7–8 мм. Голосовая функция сохранена.
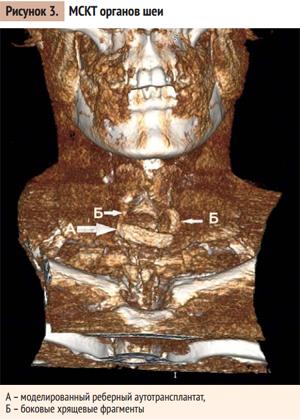 Через 6 месяцев после операции для оценки герметизации просвета гортани и трахеи, функциональной состоятельности, исключения рубцовых изменений и лизиса хрящевой ткани проводилась мультиспиральная компьютерная томография (МСКТ) органов шеи, спирометрия, видеофиброларингоскопия, ларингостробоскопия. По данным МСКТ от 25.09.2017 – состояние после неоднократных хирургических вмешательств на гортани, отмечается визуализация хрящевого аутотрансплантата. Полукруглая форма аутохряща не претерпела изменений и не лизировалась за период наблюдения (рис. 3). По данным спирометрии: вентиляционная функция дыхательных путей не нарушена.
Через 6 месяцев после операции для оценки герметизации просвета гортани и трахеи, функциональной состоятельности, исключения рубцовых изменений и лизиса хрящевой ткани проводилась мультиспиральная компьютерная томография (МСКТ) органов шеи, спирометрия, видеофиброларингоскопия, ларингостробоскопия. По данным МСКТ от 25.09.2017 – состояние после неоднократных хирургических вмешательств на гортани, отмечается визуализация хрящевого аутотрансплантата. Полукруглая форма аутохряща не претерпела изменений и не лизировалась за период наблюдения (рис. 3). По данным спирометрии: вентиляционная функция дыхательных путей не нарушена.
ЗАКЛЮЧЕНИЕ
Таким образом, в нашей клинике разработан, апробирован и внедрен в практику новый метод создания каркасного материала для пластического закрытия дефекта гортани и трахеи с применением моделированного аутохряща с помощью высокоэнергетического лазерного воздействия.
Новый метод позволяет восстановить анатомическую целостность дыхательных путей, обеспечить надежную герметизацию просвета и высокую функциональную состоятельность гортани и трахеи на заключительном этапе хирургического лечения. В работе экспериментально и клинически доказано, что новый способ предотвратит лизис хрящевого аутотрансплантата и процесс рубцевания подлежащей ткани в послеоперационном периоде.
Пластика ларинготрахеальных дефектов моделированным реберным аутохрящом позволит снизить число послеоперационных осложнений в сравнении с пластикой таких дефектов по классической методике без применения каркасного материала, способствуя улучшению качества жизни больных с хроническими стенозами гортани и трахеи.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов в ходе написания данной статьи
ЛИТЕРАТУРА
1. Паршин В.Д. Хирургия рубцовых стенозов трахеи. М.: Медицина, 2003. 152. Parshin VD. Surgery of cicatricial stenoses of the trachea.M.: Medicine, 2003. 152.
2. Каримова Ф.С., Кирасирова Е.А. Использование биоматериала Аллоплант и гемостатического материала Сержисел в реконструктивной хирургии гортани и трахеи. Вестник оториноларингологии, 2007, 5: 33-34./Karimova FS,Kirasirova EA. Use of biomaterial (cartilage) alloplant and hemostatic material sergisel in reconstructive surgery of the larynx and trachea. Vestnik Otorinolaringologii, 2007, 5: 33-34.
3. Okada K, Murakami Y, Ikari T, Haraguchi S,Maruyama T, Tateno H. Surgical treatment of
laryngotracheal stenosis by a trough technique.Auris Nasus Larynx, 1985, 12(2): 78-80.
4. Симонов С.В. Пластика зияющих дефектов трахеи на заключительном этапе хирургической реабилитации больных хроническими стенозами гортани и трахеи. Автореф. дис. канд. мед. наук. СПб., 2012. /Simonov SV. Plasticity of gaping tracheal defects at the final stage of surgical rehabilitation of patients with chronic stenosis of the larynx and trachea. Extended abstract of dissertation of PhD in medicine. St. Petersburg, 2012.
5. Богомильский Р.Д. Применение марлекса при пластическом устранении трахеостом у детей. Вестник оториноларингологии, 1968, 5: 85-89. /Bogomilsky RD. The use of Marlex in plastic removal of tracheostom in children. Vestnik Otorinolaringologii, 1968, 5: 85-89
6. Fitzgerald PG, Walton JM. Intratracheal granuloma formation: a late complication of marlex meshes splinting for tracheomalacia. Journal of Pediatric Surgery, 1996, 31(1): 1568-1569.
7. Swift EA, Grindlay JH, Clagett ОT. The repair of tracheal defects with fascia and tantalum mesh. Journal Thoracic Surgery, 1952, 24(5): 482-192.
8. Hirano M, Yoshida Т, Sakaguchi S. Hydroxylapatite for laryngotracheal framework reconstruction. Ann. Otol. Rhinol. Laryngol, 1989, 98(9): 713-717.
9. Свистушкин В.М., Старостина С.В., Селезнева Л.В. Опыт экспериментальных исследований в пластике дефектов гортани и трахеи (литературный обзор и собственный опыт). Медицинский совет, 2017, 8: 108-110. /
Svistushkin VM, Starostina SV, Selezneva LV. Experimental studies of the plasticity of larynx and trachea defects (literary review and own experience). Meditsinsky Sovet, 2017, 8: 108-110.






